AbstractPURPOSEThis study is to investigate the effects of treadmill exercise on iron accumulation and microglial cell activity in the cerebral cortex of APP-C105 transgenic Alzheimer’s mice.
METHODSThe transgenic mice and their comparative non-transgenic mice at 24 months of age were divided into 3 groups: NTC (Non-Tg-Con, n=7), TC (Tg-Con, n=7), TE (Tg-Exe, n=7). TE group ran on the treadmill (30 min/day, 5 day/week) for 8 weeks.
RESULTSThe results show that treadmill exercise significantly improved spatial memory and cognitive function in TE group compared with TC group in Morris water-maze test and Passive avoidance test. In addition, TE group with treadmill exercise showed to decrease significantly in the accumulation level of iron, amyloid-beta protein, activated-microglia factor and pro-inflammation factor in comparison with TC group. anti-inflammation factor TE group was significantly increased than TC group.
서 론철(iron)은 모든 유형의 세포에 필수적인 요소로 산소운반, 미토콘드리아의 에너지 생산과 DNA 합성 등의 역할을 한다[1]. 정상적인 뇌의 기능에서 철의 항상성(iron homeostasis)은 엄격하게 조절된다. 세포에서 자유 철(Free iron)은 다양한 철 조절 단백질들로 조절되며, 그 중 페리틴(ferritin)은 Fe²⁺를 Fe³⁺로 전환시키며 Fe³⁺를 페리틴의 내부로 저장시키는 단백질이다[2]. 이러한 페리틴의 화학적 교환은 세포 내 labile iron pool (LIP)에서 이루어지지만 비결합된 철은 산화환원반응인 펜톤반응(Fenton reaction)에 의해 일어나 반응산소종(reactive oxygen species)를 발생시키며, 반응산소종의 과도한 생산은 인체에 부정적인 영향을 준다고 보고되고 있다[3,4]. Muller et al. [5]의 연구에서 과량의 반응산소종은 심부전증, 노화, 근육 대사 장애 및 근육 피로 등을 유발한다고 보고하였다. 또한 뇌에서의 철 대사장애는 비결합된 자유철의 증가로 산화적 스트레스를 유발하여, 신경세포사멸 및 노화를 촉 진시키고 지질과산화와 단백질변형 뿐만 아니라 DNA 손상에도 관여한다[6].
최근 알츠하이머질환(Alzheimer’s disease), 파킨슨질환(Parkinson’s disease), 다발성경화증(Multiple sclerosis) 등 다양한 신경퇴행성질환에서 비정상적인 단백질들 주위에 철의 과잉이 발견되어 뇌신경과학에서 철 대사에 대한 관심이 높아지고 있다[7-9].
알츠하이머 질환은 점진적인 기억력 감소 및 인지기능 저하를 나타내며, 대표적인 특징으로 대뇌피질과 해마에서 세포 내 신경섬유원 농축(neurofibrillary tangle)과 세포 외 아밀로이드-베타의 침적이 나타나 알츠하이머 질환을 유발하는 병리기전으로 알려져 있다[10-12].
Salvador et al. [6], Everett et al. [10], Jack et al. [13]과 Kim et al. [14]은 알츠하이머 질환자의 뇌에서 철의 침적이 아밀로이드-베타의 응집을 유도하여 아밀로이드-베타 침적과 철의 연관성을 보고하였다. 또한 Meadowcroft et al. [15]은 알츠하이머 질환의 뇌 피질 조직에서는 전반적으로 아밀로이드 플라크와 페리틴이 함께 관찰되며 이는 철의 침적이 아밀로이드-베타의 변화에 영향을 미치는 것으로 제시하였다.
뇌에서 아밀로이드 플라크의 침적은 다양한 스트레스로 인하여 인체에 악영향을 준다. 아밀로이드 플라크와 아밀로이드 전구 단백질은 신경염증의 병리적 기전에 중요한 역할을 한다. 신경아교세포 중 미세아교세포는 뇌의 면역계에서 대식세포로 알려져 있다[16]. 미세아교세포의 활성이 일어나면 두 가지 역할을 하는데 초기에는 손상을 최소화하기 위해 오토파지(Autophagy) 기능으로 아밀로이드-베타를 제거하여 회복 기능을 수행하지만 지속적인 미세아교세포활성은 전염증성 사이토카인인 인터류킨-1베타(Interleukin-1 beta)와 종양괴사인자 알파(Tumor necrosis factor alpha) 등의 생산을 증가시킨다[17,18]. 증가된 인터류킨-1베타와 종양괴사인자 알파는 신경염증을 이끌어 신경세포사멸을 유도하게 된다. 특히, 아밀로이드-베타와 아밀로이드 전구체 단백질은 미세아교세포를 활성화시켜 알츠하이머 질환에서 신경염증 기전에 중요한 목적을 하는 것으로 보고되고 있다. 많은 선행연구에서 알츠하이머 질환자와 알츠하이머 질환 모델 동물의 뇌에서 미세아교세포의 활성이 나타났으며, 전염증성 사이토카인인 종양괴사인자-알파, 인터류킨-1베타, 인터류킨-1알파가 증가됨을 보고하였다[17-21]. 또한, 미세아교세포의 활성으로 인한 신경염증은 그 자체로 미세아교세포를 활성화시킬 뿐만 아니라 아밀로이드-베타의 생성을 유도시킬 수 있다[17,18].
현재 알츠하이머 질환에 대한 예방 및 치료를 위해 다양한 기전 연구가 전개되고 있으나 대부분 연구들은 약물 처치에만 의존하고 있는 실정이다. 이러한 한계점을 해결하기 위해 비약리적 방법으로 운동이 최근 관심을 받고 있으며 뇌질환에 대한 긍정적인 효과가 있다는 연구 결과들이 제시되고 있다. 지속적인 운동은 뇌의 신경보호 및 신경 복원 작용에 도움을 주며 동물 실험에서 운동은 인지기능을 향상시키고 노화된 뇌의 기억력 저하를 예방하는 것으로 나타났다[22-24].
Kortas et al. [25]은 노인 여성을 대상으로 12주간 유산소운동을 시킨 결과 혈청 페리틴 농도가 감소함을 보고하였고, Dao et al. [26]은 알츠하이머 질환 동물에게 트레드밀 운동을 실시한 결과 인지 장애와 아밀로이드 감소 뿐만 아니라 미세아교세포의 활성을 억제하였다고 보고하였다. 하지만 알츠하이머 질환의 뇌에서 철의 축적과 미세아교세포 활성화에 관련하여 운동을 통해 확인한 연구는 전무한 실정이다. 이번 연구를 통해 운동이 철의 축적과 미세아교세포 활성화를 예방하고 이를 통하여 신경 퇴행을 조절 및 지연시킬 수 있을 것으로 판단된다.
따라서 본 연구는 트레드밀 운동이 알츠하이머 질환의 뇌에서 인지능력과 철의 축적, 아밀로이드-베타의 수준, 미세아교세포의 활성화인자인 Iba-1와 신경염증유발인자인 인터류킨-1베타, 인터류킨-10, 종양괴사인자-알파의 활성 변화를 분석하고자 한다.
연구 방법1. 실험 동물본 연구는 실험을 실시하기 전에 K대학교 동물실험윤리위원회의 승인을 얻은 후 진행하였다. 실험동물은 24개월 된 알츠하이머 질환모델 마우스(APP-C105 transgenic mouse, male)를 식약처에서 제공받아 K대학교 동물사육실(습도 50±5%, 온도 22±2°C, 명암주기 12시간)에서 식이량과 물은 자유 공급하여 사육하였다. 실험동물은 비교집단(Non-Tg-Con, NTC; n =7), 알츠하이머 집단(Tg-Con, TC; n =7), 알츠하이머 운동집단(Tg-Exe, TE; n =7)으로 구분하였다.
2. 운동 방법Tg-Exe 집단은 실험동물용 DJ2-242 (Model: DJ2-242, Dual Treadmill) 트레드밀을 이용하여 운동을 실시하였다. 사전 적응훈련(경사도 0%, 운동시작 5분 2 m/min, 다음 5분 5 m/min, 마지막 20분 8 m/min)은 1주간 실시하였다. 사전 적응훈련을 시킨 후 본 운동은 주 5일, 8주간 실시하였고 저강도 운동방법으로 운동시작 5분 동안 8 m/min로, 다음 5분은 11 m/min로, 마지막 20분은 14 m/min 속도로 유지하고, 경사도는 0%로 고정하였다. Choi et al. [23], Cho et al. [27]과 Kim et al. [28]의 운동프로그램을 바탕으로 실시하였다.
3. 분석방법1) 기억력 행동검사(1) 수중미로 검사(Morris water-maze test)알츠하이머 형질전환 마우스를 대상으로 Morris water-maze test를 실시하여 표적 분면 시간(target quadrant time), 표적을 지나간 횟수(Number of crossing platform) 및 수영패턴(swimming pattern)은 컴퓨터 프로그램(SMART-LD)으로 작동하는 카메라로 측정하였고 SMART-CS program (Panlab, Barcelona, Spain)을 활용하여 분석하였다. Morris water-maze test는 원형수조(높이 40 cm×지름 1.5 m)에 수면에서 1 cm 정도 낮게 지름 12 cm인 표적(target)을 원형수조바닥에 설치하고 물(22°C-25°C)을 받아 탈지분유를 풀어 표적을 보이지 않도록 하고 검사는 처음 5일 동안 각 2회씩 지정된 출발점에서 시작하고 표적에 도달할 수 있도록 훈련시켰다. 2회 모두 표적을 찾지 못한 마우스에게는 표적의 위치를 인지시켰다. 각각의 검사는 최소 5분의 간격을 두었으며 마지막 6일째 표적을 없애고 출발지점에서 시작하여 1분 동안의 결과를 실험 데이터로 이용하였다.
(2) 수동회피검사(passive avoidance test)수동회피실험 장치의 전실은 빛을 비추어 주는 백색의 밝은 상자(18×18×25 cm), 후실은 검은색의 어두운 상자(18×18×25 cm)로 구성되어 있고, 어두운 공간의 바닥에는 전기충격을 가할 수 있는 강철 스테인리스를 설치하였다. 전실과 후실 사이의 벽에는 아래 부분에 직격 4cm되는 원형 구멍이 뚫려 있고 이 구멍은 기요틴(guillotine)형의 문으로 개폐된다. 실험동물을 한 마리씩 다른 cage에서 1분간 방치한 후, 전실에 넣고 10초간 적응을 시킨 후 기요틴형 문을 올려서 실험동물이 자유롭게 다니도록 하였다. 실험동물의 네 발이 어두운 후실로 모두 들어가면 문을 재빨리 닫고 전실에서 후실로 들어가는데 걸린 시간(initial latency time)을 측정하고 전기충격(0.5 mA)을 2초간 주었다. 그리고 5초가 지난 후에 실험동물을 꺼내 사육장 cage에 넣어주었다. 72시간 후 동일한 방법으로 실시하여 전실에서 후실로 들어가는 시간(latency to enter dark)을 최대 300초까지 기록하였다.
2) 조직 준비8주간 운동과 행동검사를 수행한 후, 동물용 Chamber를 이용하여 CO2가스를 흡입시켜 마취시킨 후, 뇌 조직을 적출하여 분석 시까지 -80℃에서 냉동 보관하였다.
3) 조직 고정8주간 트레드밀 운동과 운동기능검사를 수행한 후 western blot, 면역조직화학염색 분석을 위해 집단 당 western blot 5마리, 면역조직화학염색 2마리씩 구분하였다. Western blot을 위한 뇌 조직 적출은 동물용 chamber를 이용하여 CO2가스를 흡입시켜 마취한 후, 단백질 발현 측정을 위한 뇌 조직을 적출하였고 분석하기 전까지 -80℃ 초저온냉동고에 보관하였다. 면역조직화학염색 분석을 위해 동물용 chamber를 이용하여 CO2가스를 흡입시켜 마취한 후, 흉강을 열어 좌심실을 통해 50 mM 인산염 완충 식염수(phosphoate buffer saline, PBS)를 3분 동안 주입하고, 4% paraformaldehyde (PFA)를 0.1 M 인산 완충액에 녹인 고정액으로 10분 동안 관류시켰다. 관류 고정 후 뇌를 적출한 후, 4% PFA 고정액에 담아서 4°C에서 12시간 침전시켜 고정한 후 조직을 30% Sucrose 용액에서 5일 동안 침전시킨 다음 freezing microtome을 사용하여 40 μm 두께의 연속관상 절편을 제작하였다.
4) Western blot analysis단백질을 추출하기 위해 액화질소과 막자사발을 이용하여 단백질을 파쇄하고 단백질과 Protein Extaction Solution-RIPA를 혼합하고 균질화하여 원심분리기(Micro-centrifuge, 5417R, Eppendorf)를 이용해 원심분리(14,000 rpm, 30분, 4°C)하여 상층액을 얻었다. 5% stacking gel (3DW, 30% acrylamide: bisacrylamide, 1 M tris pH 6.8, 10% SDS, TEMED, 10% Ammonium persulfate)과 12%의 separating gel (3DW, 30% acrylamide: bisacrylamide, 1.5 M tris pH 8.8, 10% SDS, TEMED, 10% Ammonium persulfate)을 SDS-PAGE에 사용하였다. 원심분리기를 이용하여 얻은 상층액과 2X Sample loading buffer (60 mM tris pH 6.8, 25% glycerol, 2% SDS, 14.4 mM 2-mercaptoethanol, 0.1% Bromophenol blue)를 1:1 비율로 혼합한 후에 95°C에서 10분간 끓여 단백질을 변성시킨 다음에 10분간 아이스에서 cooling하고, spin down하였다. Protein size marker (ELPIS biotech, Korea)와 각 샘플들을 Mini-Protein II dual-slab apparatus (Bio-Rad, CA, USA)에 준비된 stacking gel well에 각 샘플을 분주하여 80 V로 바닥에 내려올 때까지 전기영동하였다. MeOH에 Polyvinylidine difluoride (PVDF) membrane을 적셔 activation시킨 후에 Transfer buffer (190 mM glycine, 50 mM Tris-base, 0.05% SDS, 20% methanol)로 washing하였고 Transfer buffer에 적신 whatman 3 M paper를 차례대로 겹쳐 Mini trans-bolt cell (Bio-Rad, CA, USA)에 장치한 후 200 mA로 90분 전사하고 membrane으로 증착이 끝나면 platform shaker 위에서 BSA용액(in TBS-T: 10 mM tris-base pH 8.0, 150 mM NaCl, 0.1% Tween-20)으로 60분 동안 membrane을 3% Blocking하였다. 본 실험에 사용한 1차 항체는 β -Amyloid (Santa cruz, 1:1,000), Iba-1 (Santa cruz, 1:1,000), IL-1β (Santa cruz, 1:1,000), TNF-α (Santa cruz, 1:1,000), IL-10 (Santa cruz, 1:1,000) 등을 사용하였다. 1차 항체는 3% BSA 용액에 1:1,000으로 각각 희석시킨 후에 12시간 동안 platform shaker를 이용하여 흔들어주고 0.1% TBS-T 용액으로 10분씩 3번 세척 후 2차 항체(horseradish peroxidase-conjugated goat anti-mouse, Santa Cruz, USA; horseradish peroxidase-conjugated goat anti-rabbit, Invitrogen, CA, USA)를 3% BSA 용액에 1:5,000으로 희석시켜 60분 동안 platform shaker를 이용하여 흔들어주고 TBS-T 용액으로 10분씩 3번 세척하였다. 마지막으로 membrane을 Luminata Forte Western HRP Substrate (Millipore, USA)에 넣고 1분간 발색시킨 후 membrane은 이미지 분석 시스템(Molecular Imager ChemiDoc XRS System, Bio-Rad, USA)을 사용하여 스캔 후 Quantity One 1-D Analysis Software (Bio-Rad, USA)를 이용하여 단백질의 양을 산출하였다.
5) 면역조직화학법(Immunohistochemistry)APP-C105 형질전환 알츠하이머 마우스의 대뇌피질을 절편(40 μm)하여 사용하였으며 Antigen retrieval을 위해서 각 조직을 0.01 M Sodium Citrate buffer로 85°C에서 2시간 끊인 후 0.01 M PBS로 3번 세척하였다. 10% Normal Goat serum (ab7481, abcam, UK)을 이용하여 실온에서 40분 동안 Blocking을 실시하였다. 그 후에 0.01 M PBS로 5분씩 3번 세척하였다. Blocking 후 1차 항체 amyloid-beta (sc-28365, Santa Cruz, USA)를 24시간 동안 4°C에서 Overnight시켰다. 각 조직을 0.01 M PBS로 5분씩 3번 세척 후, 실온에서 2차 항체(horseradish peroidaseconjugated Goat-mouse, Santa Cruz, USA)를 1:5,000으로 반응시켰다. 다시 0.01 M PBS로 5분씩 3번 세척 후, 실온에서 30분 동안 Vectastain-Elite ABC kit (PK-6200, Vector Laboratories, USA)의 용액으로 반응시키고 0.01 M PBS로 5분씩 3번 세척 후, DAB Peroxidase Substrate Kit(SK-4100, Vector Laboratories, USA)를 사용하여 5-8분 동안 발색하였다. 발색된 조직은 0.01 M PBS로 5분씩 3번 세척시키고 gelatin-coating된 슬라이드에 붙여 완전 건조시킨 후 80%, 90%, 100% Et-OH로 탈수시키고 80%, 90%, 100% xylene으로 투명화 시킨다. 이후 Permount를 사용하여 봉입하고 광학현미경(DM-2500, Leica Microsystems, Germany)을 통해 관찰했다.
6) 효소면역분석법(Enzyme-linked immunosorbent assay)각 집단에서 철의 수준을 측정하기 위해 Iron assay kit (MAK025, Sigma-aldrich, USA)를 사용하였으며 샘플은 대뇌피질 조직(10 mg)을 막자사발과 액화질소를 이용하여 함께 파쇄하고 Iron assay buffer와 혼합하여 균질화 시킨 후 원심분리기(Micro-centrifuge, 5417R, Eppendorf)를 사용하여 원심분리(16,000×g, 10분, 4°C) 한 후 상층액을 얻었다. 96 well plate에 샘플과 Assay buffer를 혼합하여 100 μL를 넣었다. 그 후 각 시료에 5 μL의 Iron Reducer를 추가 후 수평 쉐이커를 사용하여 RT에서 30분간 반응을 일으킨다. 그 후 100 μL의 Iron probe를 추가적으로 넣고 다시 수평 쉐이커를 사용하여 RT에서 30분간 반응을 일으킨다. 이 과정이 끝난 후 Micropalate Reader를 이용하여 593 nm에서 흡광도를 측정하였다.
연구결과1. Morris Water-maze testAPP-C105 알츠하이머 질환 모델 생쥐를 대상으로 8주간의 트레드밀 운동이 인지능력과 행동학습능력에 미치는 영향을 수중미로검사를 통해 분석하였다(Fig. 1). 먼저, 표적분면에서 수영시간은 집단 간 유의한 차이가 있는 것으로 나타났다(F[2,18] =10.192, p =.001). NC 집단은 NTC 집단에서 비해 유의하게 감소하였고(p =.003), TE 집단은 TC 집단에 비해 유의하게 증가하였다(p=.04). 다음으로 표적을 지나간 횟수는 집단 간 유의한 차이가 있는 것으로 나타났다(F[2,18] =12.867, p =.001). TC 집단은 NTC 집단에 비해 유의하게 감소하였고(p =.001), TE 집단은 TC 집단에 비해 유의하게 증가하였다(p=.032).
2. Passive avoidance test 인지능력의 변화APP-C105 알츠하이머 질환 모델 생쥐를 대상으로 8주간의 트레드밀 운동이 인지능력과 행동학습능력에 미치는 영향을 수동회피검사를 통해 분석하였다(Fig. 2). 최초 학습에서 측정한 latency는 집단 간 통계적으로 유의한 차이가 나타나지 않았다(F[2,18] =10.304, p =.742). 72시간 후 측정한 latency는 집단 간 통계적으로 유의한 차이가 나타났다(F[2,18]=133.430, p=.001). TC 집단은 NTC 집단에 비해 유의하게 감소하였고(p =.001), TE 집단은 TC 집단에 비해 유의하게 증가하였다(p=.04).
4. 대뇌피질에서 아밀로이드-베타 발현의 변화APP-C105 알츠하이머 질환 모델 생쥐를 대상으로 8주간의 트레드밀 운동이 대뇌 피질에서 아밀로이드-베타 변화 발현에 미치는 영향을 알아보았다. 면역조직화학염색(DAB Method)으로 살펴본 결과 NTC 집단보다 TC 집단과 TE 집단에서 아밀로이드-베타의 축적이 나타났다. 특히 TC 집단의 대뇌피질에서 TE 집단보다 넓은 범위에서 축적이 이루어졌다. 아밀로이드-베타를 Western blot의 방법으로 알아본 결과 (Fig. 4), 집단 간 유의한 차이가 나타났다(F[2,18] =236.032, p=.001). TC 집단은 NTC 집단에 비해 유의하게 증가하였고(p=.05), TE 집단은 TC 집단에 비해 유의하게 감소하였다(p=.012).
6. 대뇌피질에서 Pro-inflammation cytokines의 변화APP-C105 알츠하이머 질환 모델 생쥐를 대상으로 8주간의 트레드밀 운동이 대뇌 피질에서 IL-1β와 TNF-α 변화에 미치는 영향을 알아 보았다(Fig. 6). 전염증성 사이토카인인 IL-1β (F[2,18] =55.45, p=.001)와 TNF-α (F[2,18]=18.564, p=.001)는 집단 간 유의한 차이가 있는 것으로 나타났다. TC 집단은 NTC 집단에 비해 IL-1β(p =.001)와 TNF-α(p =.001)가 유의하게 증가하였고, TE 집단은 TC 집단에 비해 IL-1β(p=.001)와 TNF-α (p=.004)는 유의하게 감소하였다.
논 의이 연구는 트레드밀 운동이 APP-C105 알츠하이머 질환 모델 생쥐를 대상으로 뇌에서 철의 침착과 미세아교세포 활성에 의해 유발된 신경염증을 완화시키는데 효과가 있는지 검증하였다.
먼저 8주간의 트레드밀 운동이 인지능력 및 행동학습능력에 미치는 영향을 알아보기 위해 수동회피검사와 수중미로검사를 실시하였다. 그 결과 알츠하이머 집단보다 알츠하이머 운동집단에서 인지기능이 향상되었음을 확인할 수 있었다. 수중미로검사에서 알츠하이머 집단이 표적분면에서의 수영시간과 표적을 지나간 횟수가 감소되었고, 알츠하이머 운동집단에서 표적분면에서의 수영시간과 표적을 지나간 횟수가 증가한 것으로 나타났다. 이러한 결과는 트레드밀 운동으로 인해 행동학습능력이 개선된 것으로 나타났다. 또한 수동회피검사에서 알츠하이머 집단이 알츠하이머 운동집단보다 어두운 공간에 있는 대기시간이 증가하였다. 이를 통해 트레드밀 운동으로 인해 인지능력이 개선된 것으로 나타났다. 이는 알츠하이머 질환 모델 동물을 대상으로 트레드밀 운동을 통해 인지능력이 향상된 선행연구 결과와 일치하였다[27,29]. 규칙적인 운동은 뇌의 가소성 및 산화스트레스에 대한 신경 내구성, 혈관 생성, 에너지 대사 및 뉴로트로핀의 합성 등의 향상으로 인해 기억력과 인지능력에 변화를 보고하였다[30-32].
최근 알츠하이머 질환자의 뇌 속에서 철 대사 장애는 뇌 위축, 세포 외 아밀로이드-베타의 축적, 신경 및 시냅스 손실, 신경염증과 산화 스트레스 등과 함께 알츠하이머 질환의 진행 및 예측에 대한 중요성이 보고되고 있다[10-12,33]. 알츠하이머 질환자의 뇌 속에서 철 침적은 펜톤반응을 일으켜 과산화수소와 같은 반응산소종의 수준을 증가시켜 아밀로이드-베타 및 신경섬유원 농축의 신경 독성을 발생시킨다. 이는 신경염증을 촉진하는 성상교세포(astrocytes)와 미세아교세포의 활성화로 뇌의 신경세포사멸이 발생하여 알츠하이머 질환을 악화시킨다[3,4,17]. 이 연구에서는 APP-C105 알츠하이머 질환 모델 생쥐를 대상으로 뇌에서 철의 침적을 분석한 결과 비교집단 알츠하이머 집단에서 유의하게 높게 나타났다. 이는 알츠하이머 질환 생쥐의 뇌에서 철의 침적을 보고한 Meadowcroft et al. [15]의 선행연구와 일치하였다. 해마와 대뇌피질에서의 철 침적은 알츠하이머 질환의 병리학적 특징이 검출 되기 전에 발생하는 것으로 관찰된다. 뇌척수액 페리틴(뇌에서 철 운반생체지표)의 증가를 통해 알츠하이머 질환 발생 위험을 예측할 수 있다고 보고되고 있다[9.33]. 또한, 알츠하이머 집단보다 알츠하이머 운동 집단에서 철의 침적이 유의하게 감소한 것으로 나타났다. 현재 운동을 통해 철의 침적 변화를 살펴본 연구는 전무한 실정이지만, Ziolkowski et al. [34]은 칼로리 제한, 규칙적인 운동과 킬레이션 요법(chelation therapy)이 철의 항상성을 조절하여 철의 침적을 감소시킨다고 보고하고 있다. 이 연구의 뇌의 철 침적 감소는 트레드밀 운동이 철 항상성을 조절하는 단백질의 기능개선으로 인해 감소된 것으로 사료된다.
아밀로이드 전구체 단백질은(APP)는 알츠하이머 질환의 주요 원인으로 아밀로이드-베타를 생성하는 경로로 진행되면 뇌의 산화적 대사 감소, 인슐린 수용체 기능 억제, 학습능력 및 기억력의 결손을 유도하고, 뇌에서의 에너지 균형을 악화시킨다[10,35]. 이 연구에서는 APP-C105 알츠하이머 질환 모델 생쥐를 대상으로 뇌에서 아밀로이드 전구체 단백질과 아밀로이드-베타 단백질을 분석한 결과는 비교집단보다 알츠하이머 집단에서 유의하게 증가하였다. 이는 Koo et al. [22]과 Games et al. [36]의 선행연구와 일치한다. 그리고 알츠하이머 집단보다 알츠하이머 운동집단에서 아밀로이드 전구체 단백질과 아밀로이드-베타 단백질은 유의하게 감소하였다. 이것은 Choi et al. [23]와 Adlard et al. [29]의 결과와 같이 트레드밀 운동으로 아밀로이드-베타의 감소가 나타났다. Radak et al. [31], Lange-Asschenfeldt et al. [32]와 Vaynman et al. [37]의 연구에서 중강도 지구성 운동은 항산화 효소, eNOS, BDNF, 신경 성장 인자, 인슐린 유사 성장 인자 및 혈관 내피 성장 인자의 생산을 증가시키고, 반응산소종의 생산과 인지기능에 관여하는 아밀로이드-베타의 농도를 감소시킨다고 보고하였다.
아밀로이드-베타의 침적은 미세아교세포의 활성화 등으로 전염증성 사이토카인의 생산을 유도한다[27,38]. 알츠하이머 질환의 초기 단계에서 활성화된 미세아교세포는 식균 작용, 제거 및 분해를 증가시킴으로써 아밀로이드-베타의 축적을 감소시킬 수 있다[16,20]. 하지만 후기 단계에서는 미세아교세포의 보호 효과를 잃고 전염증성 사이토카인을 지속적으로 생성시켜 신경염증을 유발하고, 이는 아밀로이드 전구체 단백질 수준과 아밀로이드-베타의 축적을 촉진할 수 있다[39]. 선행 연구에서 알츠하이머 질환의 원인은 다양하지만 미세아교세포의 활성에 의한 신경염증 반응은 알츠하이머 질환의 병리학적 현상에 중요한 역할을 한다. 또한, 이 연구에서 APP-C105 알츠하이머 질환 모델 생쥐를 대상으로 뇌에서 미세아교세포의 활성화 지표인 Iba-1를 확인해 본 결과, 비교집단 집단에 비해 알츠하이머 집단에서 유의하게 증가한 것으로 나타났다. 이는 Wirths et al. [40]와 Heneka et al. [41]의 선행연구들과 일치하였다. Griffin et al. [42]은 Iba-1의 증가는 전염증성 사이토카인을 증가시킨다고 보고하였다. 전염증성 사이토카인(TNF-α, IL-1β)은 비교집단 집단에 비해 알츠하이머 집단에서 증가하는 것으로 나타났고, 항염증성 사이토카인(IL-10)의 수준은 비교집단과 알츠하이머 집단에서 차이가 없었다는 점에서 Manocha et al. [43]의 연구와 일치하였다. IL-10의 결과에서 알츠하이머 집단이 비교집단과 유의한 차이가 없는 결과에 대해서는 추가 연구가 필요할 것으로 생각된다.
결론적으로, 본 연구에서 트레드밀 운동은 APP-C105 알츠하이머 질환 모델 생쥐를 대상으로 뇌에서 철의 침적을 감소함으로서 신경퇴행성 질환을 유발하는 아밀로이드-베타의 침적을 감소하여 미세아교세포의 활성을 조절해 신경염증 유발을 개선시키는데 효과적인 것으로 나타났다. 철의 침적이 알츠하이머 질환에서 아밀로이드-베타의 침적 및 미세아교세포의 활성화에 중요한 역할을 나타내지만, 뇌에서의 철 대사 메커니즘에 대한 연구는 매우 부족한 실정이다. 이에 알츠하이머 질환에서의 철 조절 단백질에 관한 후속연구가 필요할 것으로 생각된다.
결 론본 연구는 트레드밀 운동이 APP-C105 알츠하이머 질환 모델 생쥐를 대상으로 뇌에서 철 침적과 미세아교세포 활성에 미치는 효과에 대해 알아보기 위하여 알츠하이머 질환 모델 생쥐를 이용하여 트레드밀 운동을 8주간 실시하였다. 8주간 트레드밀 운동은 알츠하이머 질환 생쥐의 인지능력 및 행동학습능력을 향상시켰다. 또한, 트레드밀 운동은 알츠하이머 질환 생쥐의 뇌에서 신경퇴행성 질환을 유발하는 철과 아미로이드-베타의 침적을 감소시키고 미세아교세포의 활성을 조절해 신경염증유발을 개선시켜 알츠하이머 질환의 치료 및 예방에 효과적일 것이다.
Fig. 1.Fig. 1.(A) The effect of 8 weeks treadmill exercise on levels of target quadrant, number of crossing platform in the water maze. (B) Patterns of swimming shown in the NTC, TC, and TE mice. Values are presented as the mean±SD. 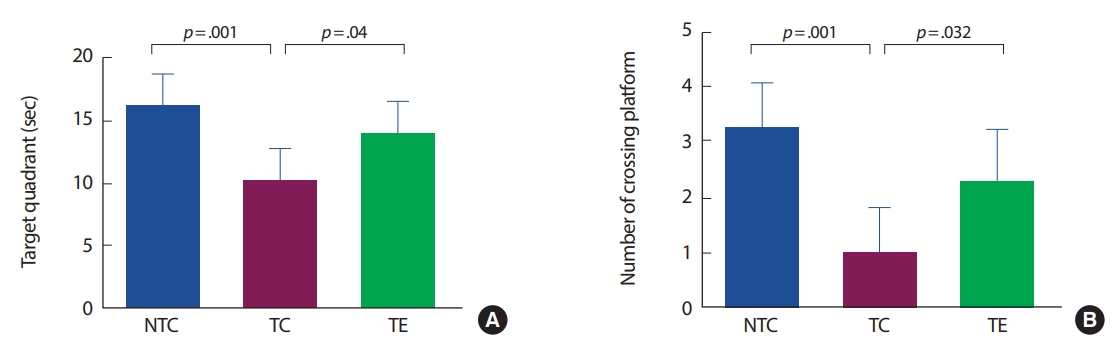
Fig. 2.Fig. 2.The effect of 8 weeks treadmill exercise on the passive avoidance test. Latency to enter the dark compartment on the training day and test day of NTC, TC, and TE mice was measured after 8 weeks of execise. Values are presented as the mean±SD. 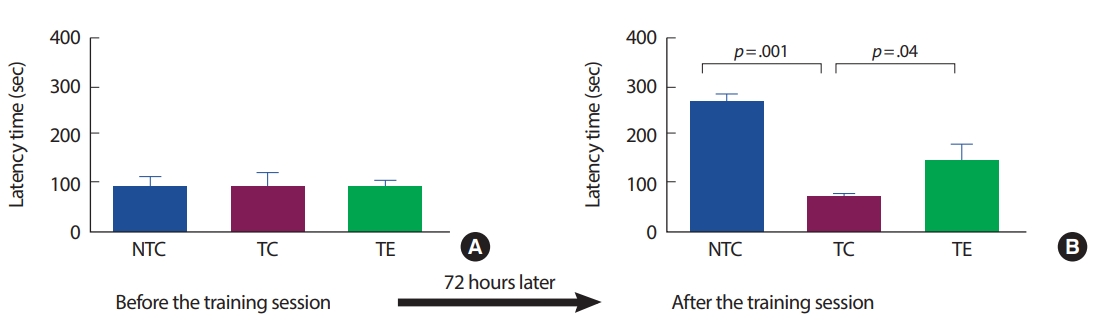
Fig. 3.Fig. 3.The effect of 8 weeks treadmill exercise on the accumulation of iron in NTC, TC, and TE mice was measured. Values are presented as the mean±SD. 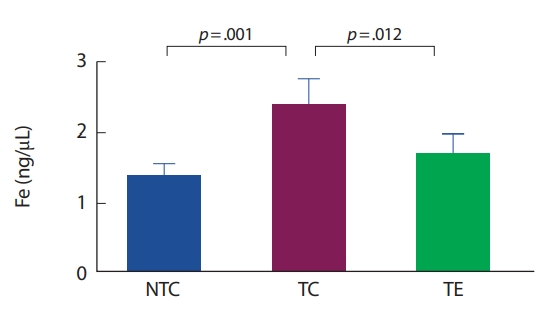
Fig. 4.Fig. 4.The effect of 8weeks treadmil exercise on Amyloid-beta in the cortex of NTC, TC and TE. (A) The aggregation of Amyloid-beta in the cortex of NTC, TC, and TE group analysed by inmunohistochemistry (DAB method). (B) The levels of Amyloid-beta in the cortex analysed by western blots. Values are presented as the mean±SD. 
Fig. 5.Fig. 5.The effect of 8 weeks treadmill exercise on level of Iba-1 in the cortex analysed by western blots. Values are presented as the mean±SD. 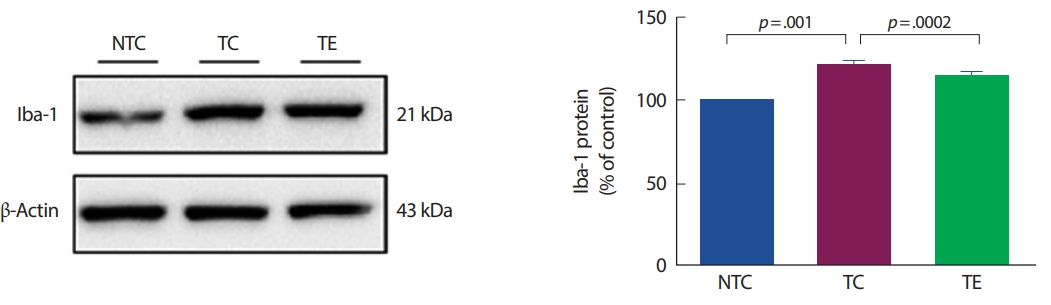
REFERENCES1. Lieu PT, Heiskala M, Peterson PA, Yang Y. The roles of iron in health and disease. Mol Aspects Med. 2001;22(1-2):1-87.
3. Smith MA, Harris PL, Sayre LM, Perry G. Iron accumulation in Alzheimer disease is a source of redox-generated free radicals. Proc Natl Acad Sci U S A. 1997;94(18):9866-8.
4. Joshi JG, Fleming JT, Dhar M, Chauthaiwale V. A novel ferritin heavy chain messenger ribonucleic acid in the human brain. J Neurol Sci. 1995;134 Suppl:52-6.
5. Muller FL, Lustgarten MS, Jang Y, Richardson A, Van Remmen H. Trends in oxidative aging theories. Free Radic Biol Med. 2007;43(4):477-503.
6. Salvador GA, Uranga RM, Giusto NM. Iron and mechanisms of neurotoxicity. Int J Alzheimers Dis. 2010;2011:720658.
8. Li K, Reichmann H. Role of iron in neurodegenerative diseases. J Neural Transm (Vienna). 2016;123(4):389-99.
9. Ayton S, Faux NG, Bush AI. Ferritin levels in the cerebrospinal fluid predict Alzheimer’s disease outcomes and are regulated by APOE. Nat Commun. 2015;6:6760.
10. Everett J, Céspedes E, Shelford LR, Exley C, Collingwood JF, et al. Ferrous iron formation following the co-aggregation of ferric iron and the Alzheimer’s disease peptide β-amyloid (1-42). J R Soc Interface. 2014;11(95):20140165.
11. Smith DG, Cappai R, Barnham KJ. The redox chemistry of the Alzheimer’s disease amyloid beta peptide. Biochim Biophys Acta. 2007;1768(8):1976-90.
12. Lee VM, and Trojanowski JQ. The disordered neuronal cytoskeleton in Alzheimer’s disease. Curr Opin Neurobiol. 1992;653-96.
13. Jack CR Jr, Wengenack TM, Reyes DA, Garwood M, Curran GL, et al. In vivo magnetic resonance microimaging of individual amyloid plaques in Alzheimer’s transgenic mice. J Neurosci. 2005;25(43):10041-8.
15. Yang QX. Cortical iron regulation and inflammatory response in Alzheimer’s disease and APPSWE/ PS1ΔE9 mice: a histological perspective. Front Neurosci. 2015;9:255.
16. Frautschy SA, Yang F, Irrizarry M, Hyman B, Saido TC, et al. Microglial response to amyloid plaques in APPsw transgenic mice. Am J Pathol. 1998;152(1):307-17.
17. Cai Z, Hussain MD, Yan LJ. Microglia, neuroinflammation, and betaamyloid protein in Alzheimer’s disease. Int J Neurosci. 2013;307-21.
18. Patel NS, Paris D, Mathura V, Quadros AN, Crawford FC, Mullan MJ. Inflammatory cytokine levels correlate with amyloid load in transgenic mouse models of Alzheimer’s disease. J Neuroinflammation. 2005;2(1):9.
19. Standridge JB. Vicious cycles within the neuropathophysiologic mechanisms of Alzheimer’s disease. Curr Alzheimer Res. 2006;3(2):95-108.
20. Qiu WQ, Walsh DM, Ye Z, Vekrellis K, Zhang J, et al. Insulin-degrading enzyme regulates extracellular levels of amyloid beta-protein by degradation. J Biol Chem. 1998;273(49):32730-8.
21. Baune BT, Konrad C, Grotegerd D, Suslow T, Ohrmann P, et al. Tumor necrosis factor gene variation predicts hippocampus volume in healthy individuals. Biol Psychiatry. 2012;72(8):655-62.
22. Koo JH, Kang EB, Oh YS, Yang DS, Cho JY. Treadmill exercise decreases amyloid-β burden possibly via activation of SIRT-1 signaling in a mouse model of Alzheimer’s disease. Exp Neurol. 2017;288:142-152.
23. Choi DH, Kwon IS, Koo JH, Jang YC, Kang EB, et al. The effect of treadmill exercise on inflammatory responses in rat model of streptozotocin-induced experimental dementia of Alzheimer’s type. J Exerc Nutrition Biochem. 2014;18(2):225-33.
24. Kim SE, Ko IG, Kim BK, Shin MS, Cho S, et al. Treadmill exercise prevents aging-induced failure of memory through an increase in neurogenesis and suppression of apoptosis in rat hippocampus. Exp Gerontol. 2010;45(5):357-65.
25. Kortas J, Kuchta A, Prusik K, Prusik K, Ziemann E, et al. Nordic walking training attenuation of oxidative stress in association with a drop in body iron stores in elderly women. Biogerontology. 2017;18(4):517-24.
26. Dao AT, Zagaar MA, Levine AT, Salim S, Eriksen JL, et al. Treadmill exercise prevents learning and memory impairment in Alzheimer’s disease-like pathology. Curr Alzheimer Res. 2013;10(5):507-15.
27. Cho JY, Hwang DY, Kang TS, Shin DH, Hwang JH, et al. Use of NSE/ PS2m-transgenic mice in the study of the protective effect of exercise on Alzheimer’s disease. Journal of Sports Science and Medicine. 2003;21(11):943-51.
28. Jang MH, Shin MC, Lim BV, Kim YP, et al. Treadmill exercise increases cell proliferation in dentate gyrus of rats with streptozotocin-induced diabetes. Journal of Diabetic Complications,. 2003;17:29-33.
29. Adlard PA, Perreau VM, Pop V, & Cotman CW. Voluntary exercise decreases amyloid load in a transgenic model of Alzheimer’s disease. The Journal of Neuroscience. 2005;25:4217-21.
30. Paillard T, Rolland Y, de Souto Barreto P. Protective effects of physical exercise in alzheimer’s disease and parkinson’s disease: a narrative review. J Clin Neurol. 2015;11(3):212-9.
31. Sarga L, Koltai E, Atalay M, Ohno H, Boldogh I. Exercise plays a preventive role against Alzheimer’s disease. J Alzheimers Dis. 2010;20(3):777-83.
32. Kojda G. Alzheimer’s disease, cerebrovascular dysfunction and the benefits of exercise: from vessels to neurons. Exp Gerontol. 2008;43(6):499-504.
33. Ayton S, Faux NG, Bush AI. Association of Cerebrospinal Fluid Ferritin Level With Preclinical Cognitive Decline in APOE-ε4 Carriers. JAMA Neurol. 2017;74(1):122-5.
34. Ziolkowski W, Ziemann E, Hermann-Antosiewicz Anna, Borkowska A, Laskowski R, et al. Are the health effects of exercise related to changes in iron metabolism? Med J Nutrition Metab. 2014;33-43.
35. Kim BK, Shin MS, Kim CJ, Baek SB, Ko YC, et al. Treadmill exercise improves short-term memory by enhancing neurogenesis in amyloid beta-induced Alzheimer disease rats. J Exerc Rehabil. 2014;10(1):2-8.
36. Games D, Adams D, Alessandrini R, Barbour R, Berthelette P, et al. Alzheimer-type neuropathology in transgenic mice overexpressing V717F beta-amyloid precursor protein. Nature. 1995;373(6514):523-7.
37. Vaynman S, Ying Z, Gomez-Pinilla F. Hippocampal BDNF mediates the efficacy of exercise on synaptic plasticity and cognition. Eur J Neurosci. 2004;20(10):2580-90.
38. Sastre M, Klockgether T, Heneka MT. Contribution of inflammatory processes to Alzheimer’s disease: molecular mechanisms. Int J Dev Neurosci. 2006;24(2-3):167-76.
39. Karran E, Mercken M, De Strooper B. The amyloid cascade hypothesis for Alzheimer’s disease: an appraisal for the development of therapeutics. Nat Rev Drug Discov. 2011;10(9):698-712.
40. Wirths O, Breyhan H, Marcello A, Cotel MC, Brück W, et al. Inflammatory changes are tightly associated with neurodegeneration in the brain and spinal cord of the APP/PS1KI mouse model of Alzheimer’s disease. Neurobiol Aging. 2010;31(5):747-57.
41. Heneka MT, Sastre M, Dumitrescu-Ozimek L, Dewachter I, Walter J, et al. Focal glial activation coincides with increased BACE1 activation and precedes amyloid plaque deposition in APP[V717I] transgenic mice. J Neuroinflammation. 2005;2:22.
|
|
|||||||||||||||||||||||||||||||||||||