조골세포 소포체 스트레스로 인한 골 손실을 개선하기 위한 운동효과 물질이 포함된 extracellular vehicles의 효과
Abstract
PURPOSE
This study aims to investigate the bone-muscle crosstalk mechanism by treating dysfunctional osteoblasts with extracellular vehicles (EVs) containing exercise mimetics released during muscle contraction, with the intention of identifying key factors in regulatory mechanisms.
METHODS
To understand the bone-muscle crosstalk mechanism, the effects of treatment were evaluated in osteoblasts and C2C12. First, palmitate was administered to osteoblasts to induce bone loss due to endoplasmic reticulum (ER) stress. For validation, two groups were evaluated: a control group (CON) and the palmitate treatment group (PAL). Then, C2C12 myotubes were stimulated with electrical pulses to induce muscle contraction, and the released extracellular vehicles (EVs) were harvested and applied to osteoblasts. The results were used to determine the relevant mechanisms for improving bone loss. The impact of EVs released from muscles on osteoblasts was examined using the CD63-GFP plasmid. Four groups were used to compare across the different variables of interest: CON; EV, EV-treated group; PAL; EP, EV+palmitate-treated group.
RESULTS
The palmitate-treated osteoblasts showed increased expression of inositol-requiring protein 1α (IRE1α), decreased sarcoplasmic/endoplasmic reticulum Ca2+-ATPase (SERCA), reduced ER Ca2+, and mitochondrial membrane potential (MMP), indicating induced ER stress. Palmitate-induced ER stress was associated with elevated nuclear factor kappa B (NFκB) and receptor activator of NFκB (RANKL) levels and an increased RANKL/osteoprotegerin (OPG) ratio, causing bone loss. The treatment of osteoblasts with EVs from muscle contraction was found to improve ER stress, the levels of ER Ca2+, MMP, NFκB, and RANKL, and the RANKL/OPG ratio.
CONCLUSIONS
Palmitate reduces ER Ca2+ and induces osteoblast ER stress while impairing mitochondrial function. Furthermore, through the RANKL/RANK/OPG pathway, a key mechanism related to bone loss is induced. However, substances induced by muscle contraction can act on osteoblasts through exosomes, potentially improving this process.
Keywords: Bone, Muscle, Endoplasmic reticulum, Bone loss, Exosome
색인어: 뼈, 근육, 소포체스트레스, 골 손실, 엑소좀
서 론
고지방 식이[ 1]와 노화 및 폐경[ 2] 등에 따른 골 손실의 경우 체지방 증가에 따른 지방 세포에서의 염증성 사이토카인의 과잉 분비가 파골세포와 조골세포의 불균형이 하나의 원인으로 지목되고 있다. 특히 지방산 중 palmitate와 같은 포화지방산은 골격근 세포를 비롯한 다양한 세포에서의 endoplasmic reticulum (ER) stress의 원인이 된다[ 3, 4]. 조골세포에서의 ER 스트레스 유도는 조골세포의 분열과 미네랄 침착을 억제할 뿐 아니라 골 손실을 야기한다[ 5]. 이러한 골 손실을 개선하기 위한 방법으로는 웨이트 트레이닝과 줄넘기 등의 체중 부하 운동이 주로 제시되어 왔으며[ 6], 걷기, 수영, 사이클 등 같은 유산소운동은 상대적으로 효과가 떨어지는 것으로 인식되었다[ 7]. 그러나 최근 연구에 따르면 수영 같은 운동으로도 골 질량이 감소된 쥐에서 점프 운동만큼 효과적으로 골밀도(bone mineral density, BMD)와 골 미세구조가 개선된다[ 8]. 이러한 결과는 체중 부하 없이 근육 수축만으로도 뼈 건강을 유지하고 개선하기에 충분함을 시사한다[ 9]. 그러나 이와 관련된 bone-muscle crosstalk에 관한 명확한 기전의 이해는 많이 부족하다. 골격근 세포(C2C12)에 전기 자극으로 근수축을 유발할 경우 extracellular vehicles (EVs)의 한 종류인 microvesicles을 방출하게 된다[ 10, 11]. 이렇게 분비된 EVs에는 운동 또는 근수축에 의해 조절되는 다양한 myokine이나 미토콘드리아 효소를 조절하는 미토콘드리아 DNA (mtDNA) 등이 다량 함유되어 있다[ 10, 12]. 따라서 운동으로 인한 근수축 시 세포막에서 방출된 EVs에 포함된 다양한 운동유발물질이 호르몬과 유사하게 작용하여 신체 다양한 조직에 그 효과를 전달하고 기능을 조절하게 된다. 이에 운동으로 인한 골격근 수축으로 방출된 EVs 에 포함된 운동유발물질(microRNA, mRNA 및 단백질 등)은 세포 내 다양한 대사 작용에 관여함을 알 수 있다. 따라서 골 손실 개선 또는 그 기전을 밝히기 위한 노력으로 중력 또는 체중부하에 따른 효과를 배제하고 순수한 근수축에 따른 운동 효과를 분석하기에 EVs는 매우 유용하게 사용될 수 있다. 이에 본 연구는 근수축에 의해 골격근으로부터 분비되는 운동유발 물질이 포함된 EVs가 조골세포 ER 스트레스에 의해 유도된 골 손실 기전의 활성에 따른 골 손실 환경이 개선되는지 분석하고자 한다. 또한 골 손실 환경 개선을 위한 조절 기전과 관련 핵심인자를 확인함으로써 뼈와 근육의 상호작용 기전을 이해하고자 한다. 이는 조골세포 ER 스트레스에 의한 골 손실 환경을 개선하기 위한 운동의 효과 중 체중부하를 제외한 순수한 근수축에 따른 효과와 그 기전을 이해하는데 도움이 될 것이다.
연구 방법
본 연구는 뼈와 근육의 상호작용 기전을 이해하기 위해 먼저 palmitate를 이용하여 조골세포 ER 스트레스를 유도함으로써 골 손실 환경을 조성하였다. 이와 함께 C2C12에 전기 자극하여 근수축을 유도한 후 방출된 EVs를 palmitate를 처치한 조골세포에 처치하여 ER 스트레스 억제에 따른 골 손실 관련 기전의 개선 효과를 분석하였다. 이를 입증하기 위한 그룹은 총 4그룹(CON, control group; EV, EVs treated group; PAL, palmitate treated group; EP, EVs+palmitate treated group)으로 분류하였다. 실험설계는 Fig. 1과 같다.
Fig. 1.
Fig. 1.Experiment design. ER, endoplasmic reticulum; EVs, extracellular vehicles; MMP, mitochondrial membrane potential; CON, control group; EV, EVs treated group; PAL, palmitate treated group; EP, extracellular vehicles+palmitate treated group. 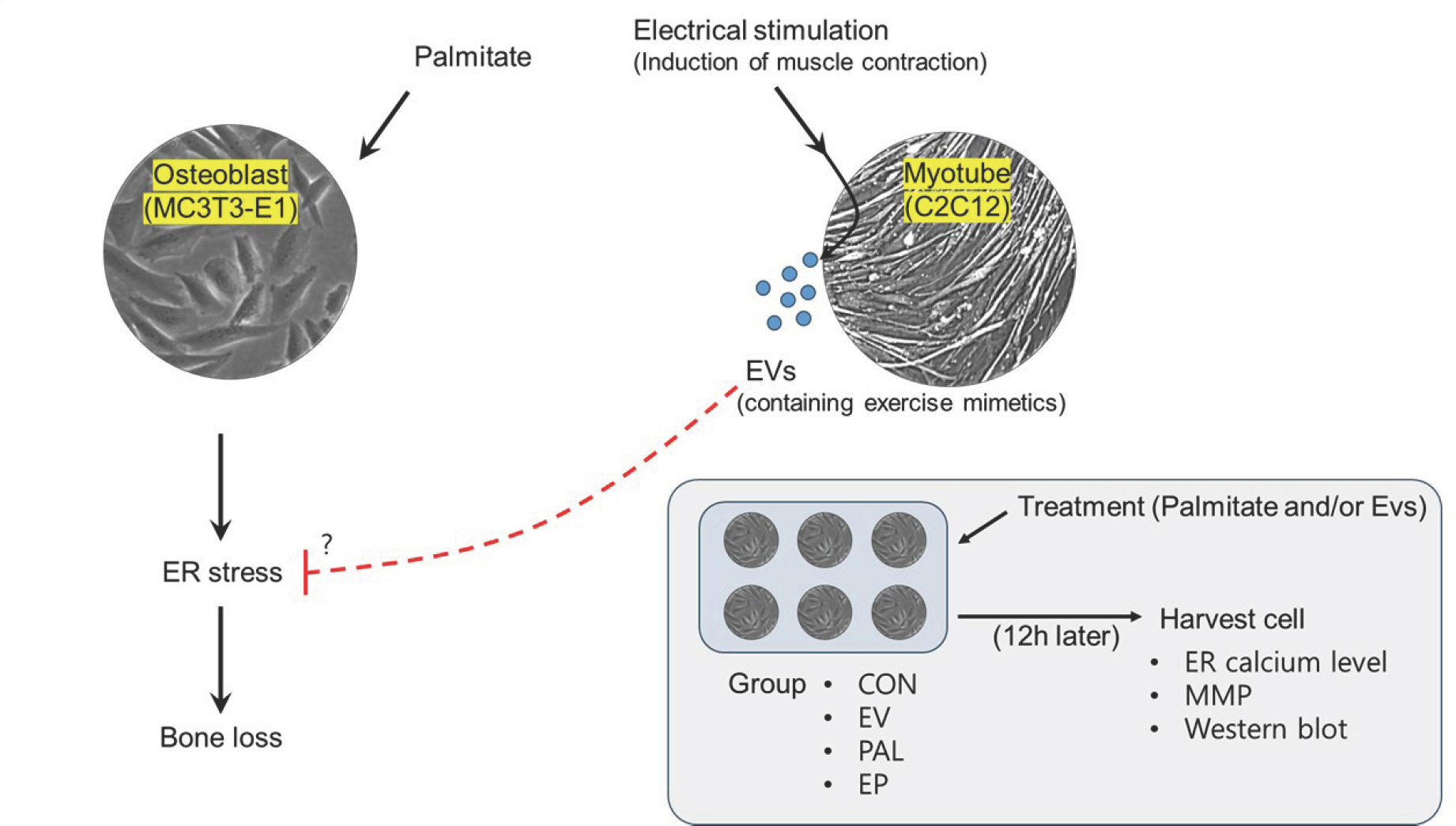
1. 골격근 세포를 이용한 운동유발
1) 골격근세포 배양
골격근 세포는 C2C12 (ATCC, USA)를 이용하였다. C2C12는 10% fetal bovine serum (Hyclone, Logan, UT), 100 U/mL의 penicillin G, 100 µg/mL의 streptomycin sulfate (Gibco, USA)를 함유하고 있는 high glu-cose Dulbecco's modified Eagle's medium (DMEM) (Welgene, Korea)으로 37°C, 5% CO2의 환경에서 배양하였다. 세포는 35 mm plate에 약 2.5×10,000 개씩 분주하고 90% 이상 자라면 배지를 제거하고 2% horse serum (Hyclone, Logan, UT)이 함유된 분화 배지로 교체하여 약 7일간 배양하여 세포가 근관세포(myotube) 모양으로 분화된 것을 확인한 후 처치를 실시하였다.
2) 전기자극에 따른 근수축 유발
골격근 세포에 운동효과를 유발하기 위해 전기자극을 통한 근수축을 유도하였다. 배양된 세포가 근관세포(myotube) 모양으로 분화된 것을 확인한 후, 근수축 유도를 위한 전기 자극은 15 cm 세포배양용 디쉬 뚜껑에 백금 선을 연결을 한 후 전기 자극기(Digitimer Ltd, Eng-land)를 이용하여 (5 Hz, 10 ms, 50 V) 강도로 2시간 동안 실시하였다. 전기 자극 동안 골격근 수축 상태를 확인하였으며, 자극 후 버퍼에 유리된 EVs (exosomes)를 채취하였다.
3) Exosome 정제
C2C12 세포로부터 회수된 DMEM buffer는 세포 및 세포 잔해(cellular debris) 제거를 위해 2,000 g, 4℃에서 20분간 원심분리하고 상층 액(supernatant)만을 분리하였다. 이후 상층액은 2차적으로 cell debris 제거를 위해 10,000 g에서 30분 동안 원심분리 되었다. 이후 exosome 을 얻기 위해 cell debris가 제거된 상층액은 초고속원심분리기(Beck-mann, USA)를 이용하여 100,000 g에서 70분 동안 원심분리 되었다. 이후 상층액을 제거하고 남은 pellet은 기타 단백질 제거를 위해 1 mL의 phosphate buffer saline (PBS)로 세척한 다음 100,000 g으로 1시간 동안 다시 원심분리 되었다. 이후 상층액을 제거한 pellet을 100 µL의 PBS로 재부유하여 최종적으로 exosome을 얻었다.
4) Exosome 라벨링을 통한 조골세포와 exosome 상호작용 확인
Exosome 및 전기 자극을 준 세포는 1X RIPA 완충액을 사용하여 lysis 되었고 20 μg의 단백질을 추출했다. 추출한 단백질은 전기 연동 법으로 단백질 발현을 측정하였으며, heat shock protein (HSP) 70 (Santacruz biotechnology, Santacruz, USA), αB-Crystallin (Santacruz biotechnology, Santacruz, USA) 및 HSP27 (Santacruz biotechnology, Santacruz, USA)항체를 이용하였으며, exosome에서 발현되지 않는 Calnexin (Santacruz biotechnology, Santacruz, USA)과 같은 세포 마커는 음성 대조군으로 사용되었다. 사용된 이차 항체는 rabbit anti-rabbit IgG conjugated secondary antibody (Santacruz biotechnology, Santacruz, USA)와 mouse IgG HRP (Santacruz biotechnology, Santacruz, USA)를 사용하였다. 또 한 가지의 Exosome 마커인 CD63은 CD63-eGFP Plasmid DNA를 lipofectamin을 이용하여 3일간 골격근 세포에서 과 발현을 유도하였으며 전기적인 자극법에 의해 방출된 exosome을 형광 현미경(NIKON, Japan)을 이용하여 조골세포에서의 부착(adhesion)을 관찰하였다.
2. 조골세포 ER 스트레스 유발에 따른 골 손실 환경 모델
1) 조골세포 배양
조골세포 내 ER 스트레스유발에 따른 골 손실 환경을 유도하기 위해 MC3T3-E1 (mouse calvarial osteoblasts) 세포를 이용하였다. MC3T3-E1 세포는 10% fetal bovine serum (FBS, GibcoBRL, USA)과 1% 항생제 (Penicillin G sodium 10,000 units/ml, streptomycin sulfate 10,000 µ g/mL and Amphotericin B 25 µ g/mL in 0.85% saline, GibcoBRL, USA)가 첨가된 α minimum essential medium (α-MEM, GibcoBRL, USA) 2 mL가 담긴 6-well plate에 적정 세포(5×104 cells/well)를 분주하였다. 이를 온도(37℃), 습도(100%), 산소(95%), 그리고 이산화탄소(5%)가 일정하게 유지되는 환경에서 배양하였다. 배양액은 세포가 충분한 증식이 일어날 때까지 2-3일 간격으로 교환하였고, 1:3의 비율로 계대 배양 하여 5-6계대 배양된 세포를 사용하였다.
2) Palmitate-BSA conjugation 처치에 따른 조골세포 내 ER 스트레스에 따른 항상성 저하
조골세포 ER 스트레스 유발은 포화지방산인 palmitate를 bovine serum albumin (BSA)을 이용하여 제조한 뒤 사용되었다. 제조는 palmitate sodium (100 mM, SIGMA)을 70°C에서 30분 동안 고압 멸균된 증류수에 용해시키는 방법으로 하였다. 이때 BSA (10%) 또한 55°C에서 30분 동안 조골세포 배지에 용해하고 여과했으며, 용해된 palmitate용액을 BSA 용액에 적가하고 사용할 때까지 −80°C에서 10 mM 농도로 보관하였다. ER 스트레스 유발을 위한 최종 농도와 시간은 200 uM로 하여 12시간 동안 처리하였다.
3) Thapsigargin을 이용한 ER Ca2+ 측정
세포 내 ER Ca2+ 수준변화를 측정하기 flou-4 AM (F14204, Thermo Fisher, USA)을 이용하여 측정하였다. MC3T3-E1 세포는 confocal dish 로 분주 되며, 50 nM/mL의 Ca2+ dye가 포함된 alpha MEM buffer로 교체된 후 약 30분 동안 incubation 되었다. 이후 새로운 Alpha MEM buffer를 이용하여, 세포 안에 흡수되지 않은 Ca2+ dye 시약이 제거되며, 이후 공초점 현미경(Confocal microscope, Nikon C1, Nikon, Japan)에서 10 μM thapsigargin을 처치하면서 형광값을 측정하였다. 세포 내 Ca2+ 산정 공식 [Ca2+]i=Kd (F-Fmin)/(Fmax-F)에 따라 세포 내 Ca2+ 수준을 판정하였으며, ER Ca2+은 상대적인 형광값을 비교하여 측정하였다. 측정에 이용되는 여기(excitation)/방출(emission) 값은 480/520 및 495/515 nm를 사용하였다.
4) 미토콘드리아 막 전압(mitochondrial membrane potential, MMP) 측정
미토콘드리아 막 전압변화를 측정하기 위해 tetramethylrhodamine, methyl ester (TMRM) dye를 이용하였다. Confocal dish에서 관모양의 MC3T3-E1 세포는 TMRM (T668, Thermo Fisher, USA) 50 nM이 함유된 αMEM buffer에 약 30분 동안 배양되었다. 이후 공초점 현미경 (Confocal microscope, Nikon C1, Nikon, Japan)에서 100 μM carbonyl cyanide m-chlorophenylhydrazone (CCCP)을 처치하면서 형광 값을 측정하였다. CCCP를 처리한 후 최고점의 형광 값과 최저점 값 사이의 차이를 막 전압으로 간주하여 측정하였으며, 최고점-최저점을 값이 높은 시료가 막전압이 높음을 나타내었다. 측정에 이용되는 여기/방출 값은 548/574 및 495/515 nm를 사용하였다.
5) ER 스트레스 인자 확인을 위한 단백질 추출 및 웨스턴블랏
단백질을 추출은 용해 완충액(Roche. Mannheim, Germany)에 prote-ase inhibitor (Roche. manheim, Germany) 함유된 용액을 첨가하여, 배양된 조골세포를 스크래퍼(scraper)로 긁은 다음 15,000 rpm에서 15분 동안 원심분리 하였다. 원심 분리된 용액 중 상층액만을 분리한 후 상층액의 2 µ L를 protein assay 용액(Bio-Rad, CA, USA) 1 mL에 첨가한 다음 분광광도계(Eppendorf, CA, USA)를 이용하여 560 nm의 흡광도에서 단백질량을 정량하였다. 정량화된 단백질에서 각 샘플당 동일한 단백질량(20 µ g)을 SDS-gel loading 용액에 총 20 µ L가 되도록 혼합한 다음 100℃에서 10분간 변성시켰다. 변성된 단백질(20 µ L)을 스탠다드 단백질 마커(SDS-PAGE molecular weight maker, Bio-rad, CA, USA)와 함께 Mini-Protein II dual-lab apparatus (Bio-Rad, CA, USA)에 의해 만들어진 10% SDS-polyacrylamide gels에 각 샘플을 주입한 다음 100 Volt에서 2시간 동안 단백질이 바닥에 닿을 때까지 전기영동 하였다. 전기 영동된 단백질을 PVDF membrane (Amersham, CA, USA)에 전이하기 위해 Mini trans-module (Bio-Rad, CA, USA)을 이용하여 전이 용액(190 mM glycine, 50 mM Tris-base, 20% methanol, .05% SDS) 속에 단백질이 전기영동된 젤과 PVDF membrane (millipore) 및 3M paper를 차례로 겹치도록 한 다음 110 Volt에서 1시간 40분 동안 전이하였다. 단백질이 전이된 membrane은 phosphate-buffered saline (PBS) (Nacl 8 g, KCl 0.2 g, Na2HPO4 1.44 g, KH2PO4 0.24 g, pH7.4)에 5% skim milk가 첨가된 용액에서 1시간 동안 rocker platform (Fine PCR, Korea)에서 blocking하였다. 그 다음 membrane은 PBS에 0.1% tween-20이 함유된 용액(PBST)에서 10분간 3번 세척하였으며, 세척된 membrane은 일차 항체인 HSP70; sarcoplasmic/endoplasmic reticulum Ca2+-ATPase (SERCA); inositol-re-quiring protein 1α (IRE1α); hypoxia-inducible factor-1α (HIF-1α); nuclear factor kappa B (NFκB); receptor activator of NFκB (RANKL); osteoprotegerin (OPG) (Santacruz biotechnology, Santacruz, USA) 첨가된 용액에서 2시간 동안 반응된 후 PBST 용액에서 1×15 min과 2×5 min 동안 세척하였다. 일차 항체에서 반응된 membrane은 rabbit anti-rabbit IgG conjugated secondary antibody (Santacruz biotechnology, Santacruz, USA)가 첨가된 용액에서 2시간 동안 반응된 다음 PBST용액에서 1×15 min과 2×5 min 동안 세척하였다. 세척된 membranes은 ECL detection reagent (Amersham, CA., USA) 용액(1 mL)에 1분간 노출된 후 Bio-Rad chemidoc XRS (Bio-rad, CA, USA)를 통해 이미지화 한 후 면역반응(immunoreactive) 밴드의 상대적 강도를 정량화 하였다.
3. 자료처리
측정된 자료는 SPSS Win 23.0 통계 프로그램을 이용하여 평균과 표준오차(standard error of mean, SEM)를 산출하였다. 조골세포에 palmitate 처치에 따른 ER 스트레스 유도 및 골 손실 환경 유무의 확인을 위한 CON과 PAL 그룹 간의 비교는 independent t-test를 실시하였다. 그 외 palmitate와 EVs 처치에 따른 모든 그룹 간 평균차이의 검증은 일원 변량분석(one-way ANOVA)을 적용하였다. 분석결과 통계적으로 유의한 차이가 있을 경우 Duncan 방식에 의해 사후검정을 실시하였다. 가설의 수락기준은 p <.05로 설정하였다.
연구 결과
1. Palmitate는 조골세포에서 ER 스트레스를 유발한다
포화지방산이 ER 스트레스를 유발하는가를 확인하기 위해 조골세포에 12시간 동안 palmitate를 처리한 결과는 Fig. 2와 같다.
Fig. 2.
Fig. 2.Palmitate induces endoplasmic reticulum (ER) stress in osteoblasts. The expression levels of IRE1α and SERCA were analyzed by Western blotting af-ter treating osteoblast cells with palmitate for 12 hours (A-C). Cumulative data of the maximum Ca2+ leakage rate (D-F) induced by thapsigargin response under normal and palmitate conditions and data of MMP fluorescent leakage rate (G-I) induced by CCCP response were assessed. ER, endoplasmic reticulum; MMP, mitochondrial membrane potential; CON, control group; PAL, palmitate treated group. *** p<.001 vs. CON. 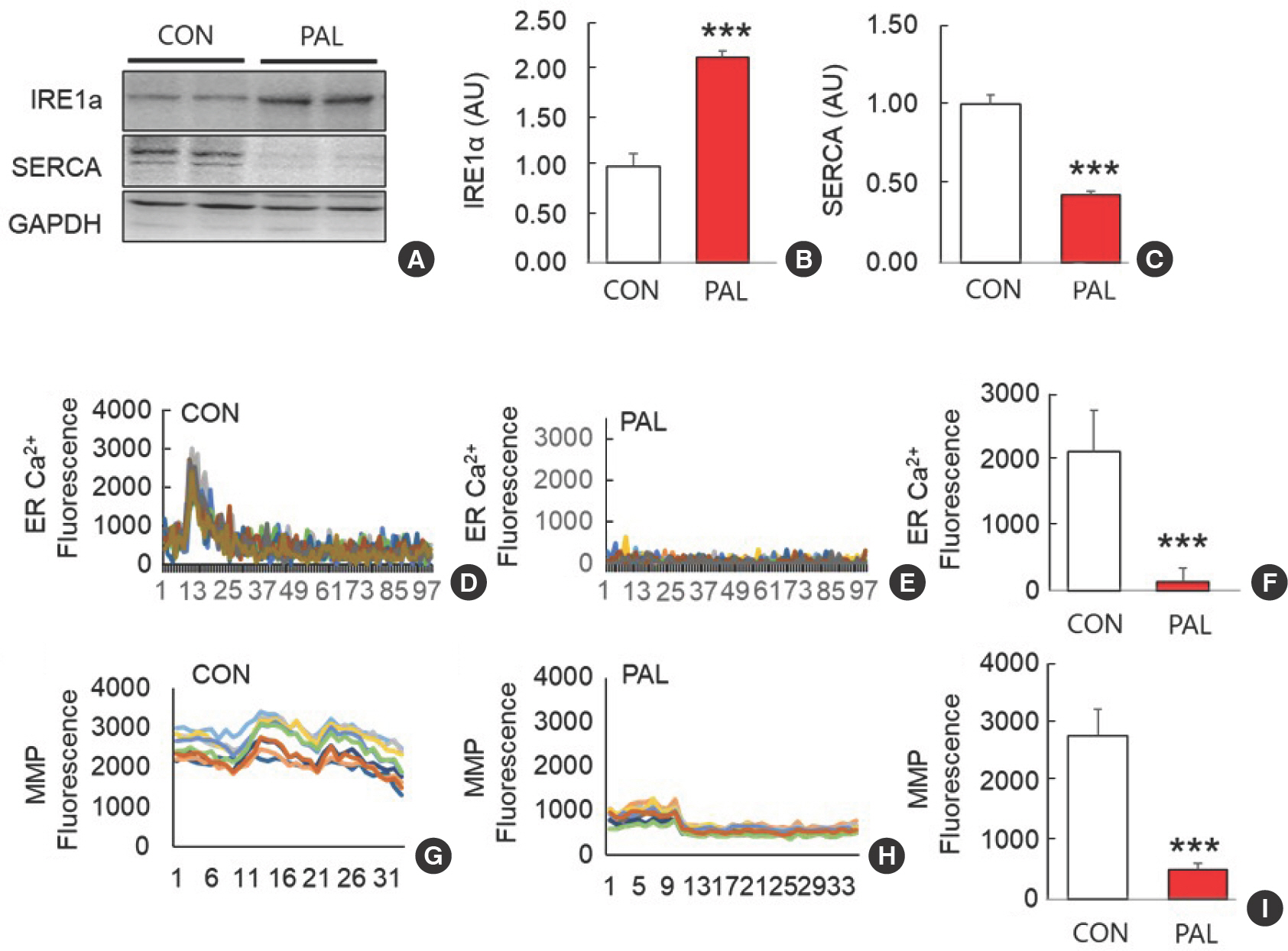
PAL의 경우 ER 스트레스 인자인 IRE1α ( Fig. 2A, B)는 CON에 비해 유의하게 ( p <.001) 증가하였고, SERCA ( Fig. 2A, C)는 유의하게 ( p <.001) 감소하였다. ER Ca 2+ level ( Fig. 2D- F)과 MMP ( Fig. 2G- I) 또한 PAL이 CON에 비해 유의하게( p <.001) 감소하였다. 이러한 결과는 조골세포에서의 palmitate 처치는 ER 스트레스를 유발함을 의미한다.
2. 조골세포 ER 스트레스 유도는 골 손실 기전을 활성한다
Fig. 2와 같이 palmitate에 의해 유도된 ER 스트레스가 골 손실관련 기전에는 어떠한 영향을 미치는가를 분석한 결과는 Fig. 3과 같다.
Fig. 3.
Fig. 3.Osteoblast endoplasmic reticulum (ER) stress induces bone loss through the NFκB and RANKL-OPG pathway. After treating osteoblast cells with palmitate for 12 hours, the expression levels of NFκB (A, B), RANKL (A, C), and OPG (A, D) were analyzed using Western blotting. Based on this analysis, the RANKL/OPG ratio (E) was calculated. CON, control group; PAL, palmitate treated group. * p<.05, *** p<.001 vs. CON. 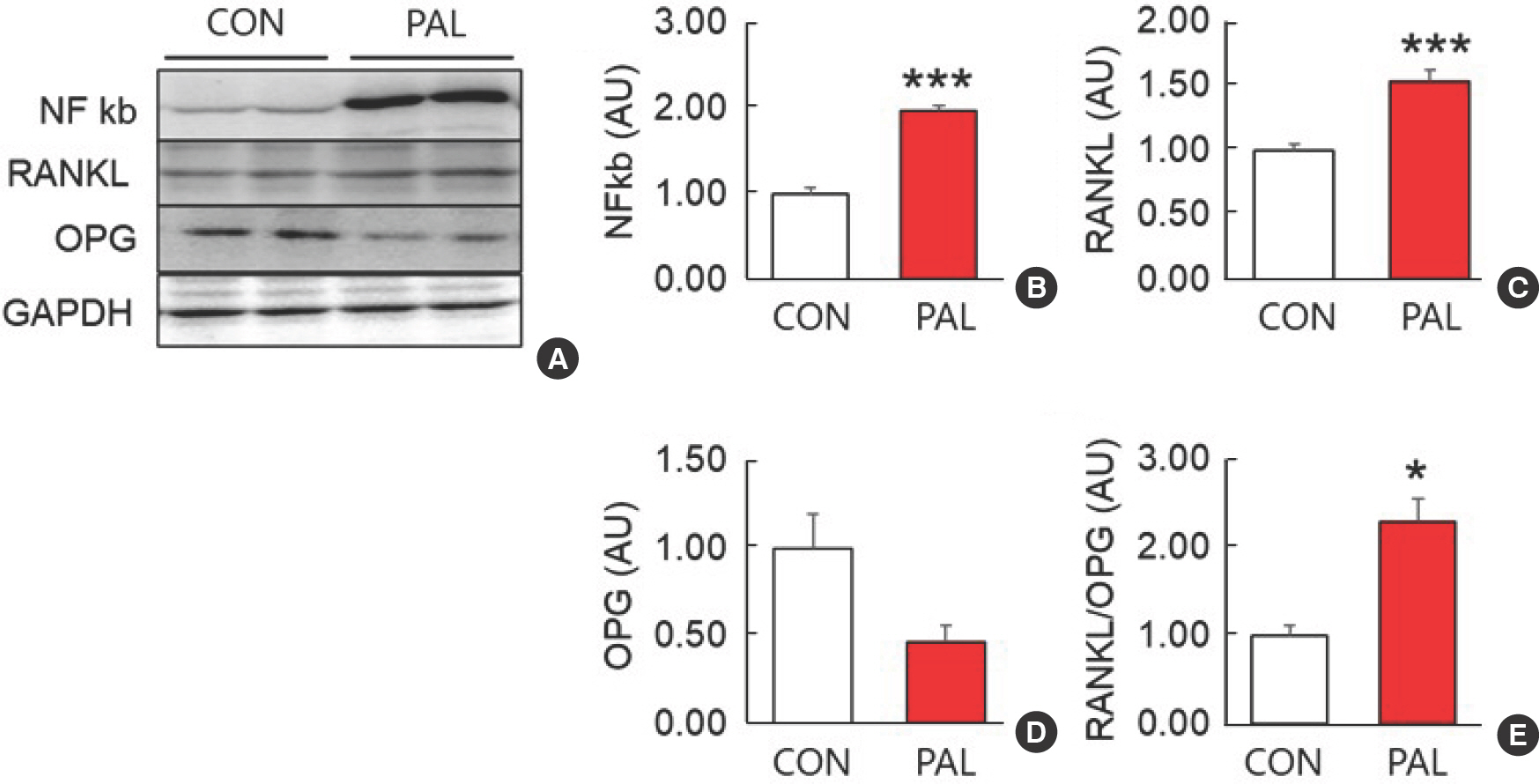
골 손실 관련 인자 중 NFκB와 RANKL은 PAL이 CON에 비해 유의하게( p <.001) 증가하였으며( Fig. 3A- C), OPG는 PAL이 CON에 비해 감소는 하였으나 두 그룹간 유의한 차이가 없었다 ( Fig. 3A, D). 그러나 RANKL/OPG ratio는 PAL이 CON에 비해 유의하게( p =.026) 높았다 ( Fig. 3A, E). 이에 palmitate에 의한 ER 스트레스는 파골세포 성숙, 뼈 모델링 및 뼈 리모델링에서의 역할로 잘 알려져 있는 RANKL/RANK/OPG pathway [ 13]를 통해 골 손실 환경을 유도함을 알 수 있다.
3. 골격근 수축에 의해 방출된 EVs는 조골세포에 작용한다
골격근 수축에 따른 운동유발물질이 골격근세포에서 방출되는지를 확인하기 위해 골격근세포에 전기자극을 유도한 후 EVs 방출유무를 확인한 결과는 Fig. 4A, B와 같다.
Fig. 4.
Fig. 4.Extracellular vehicles (EVs) released through skeletal muscle contraction induced by electrical pulse stimulation affect osteoblasts. C2C12 myotubes were subjected to electrical pulse stimulation for 2 hours, and the expression of exosome-specific proteins, HSP70 and αB-crystallin, was analyzed by Western blotting. Calnexin was analyzed as a negative control (A, B). Fluorescence microscopy was used to confirm whether the CD63-GFP plasmid trans-fected into C2C12, which secretes exosomes from skeletal muscle, binds to osteoblasts. The expression of GFP in osteoblasts was examined to verify the binding (C). 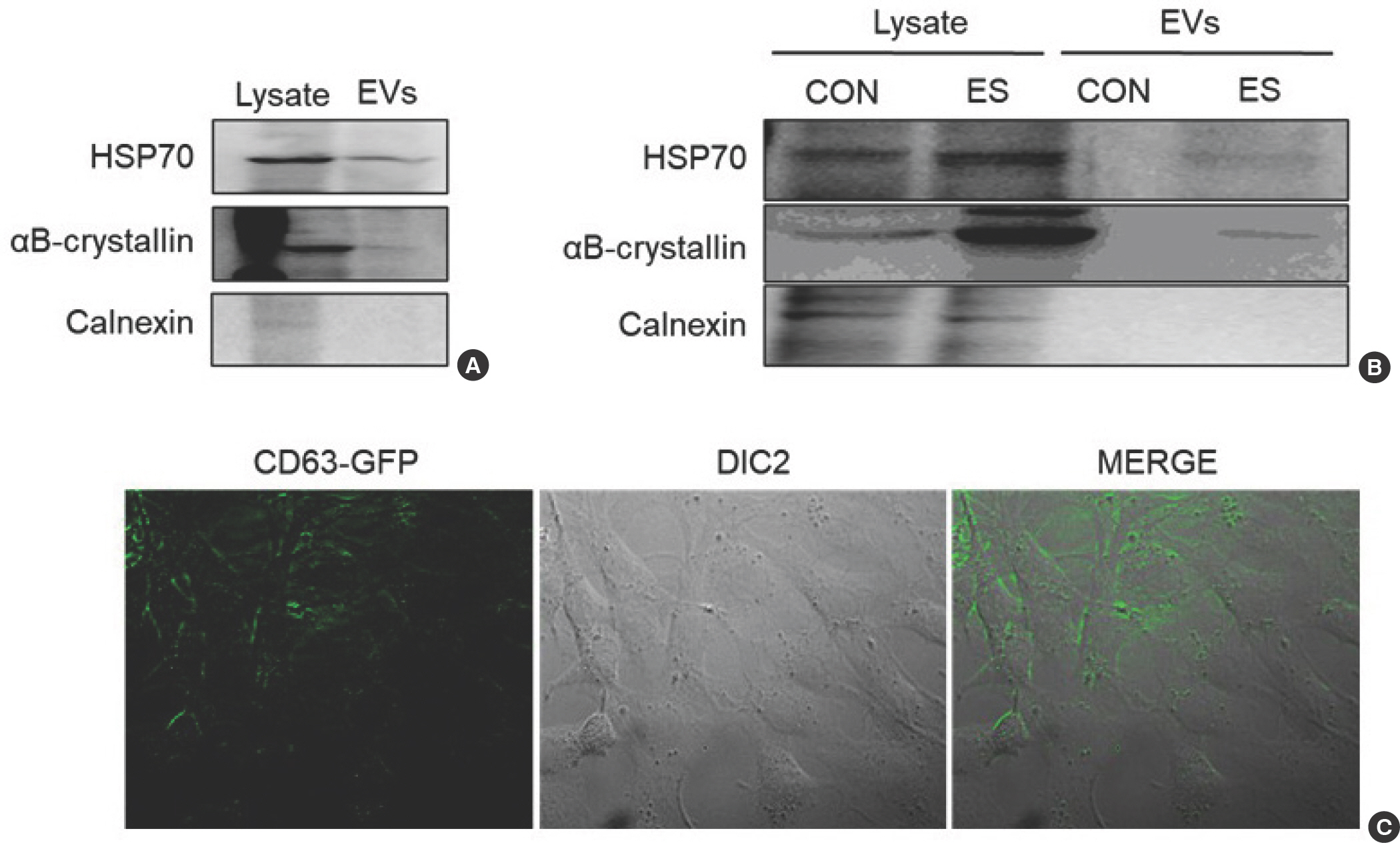
골격근 세포에 전기자극을 유도한 후 방출된 EVs추출 유무를 확인한 결과 exosome에 존재하는 단백질인 HSP70과 αB-crystallin이 발현됨을 확인하였다. 또한 exosome 비 특이 단백질인 calnexin은 발현되지 않음을 확인하였다( Fig. 4A). 이와는 반대로 전기 자극을 실시하지 않은 골격근 세포에서 분리된 exosome에서는 HSP70과 αB-crystallin의 발현은 확인할 수 없었다( Fig. 4B). 전기자극에 의해 골격근 세포에서 방출된 exosome이 조골세포에 작용하는가를 확인하기 위해 exosome에 존재하는 단백질인 CD63에 GFP를 결합시킨 CD63-GFP를 조골세포에 처치한 결과 GFP가 조골세포에 결합하고 세포 내 침투한 것을 형광현미경을 이용하여 확인하였다( Fig. 4C). 이러한 결과는 골격근 수축에 의해 방출된 EVs는 뼈로 이동하여 조골세포에 작용함을 의미한다.
4. Palmitate 유도 조골세포 ER 스트레스에 따른 골 손실 환경은 근수축에 의해 개선된다
조골세포에 골격근세포 수축에 의해 방출된 EVs를 처치한 결과는 Fig. 5와 같다. CON과 EV 간에는 ER 스트레스 관련 인자의 변화는 없었다( Fig. 5A, E). 그러나 PAL의 경우 CON에 비해 IRE1α ( Fig. 5A, C)는 유의하게 증가하였다( p =.001). 그에 비해 SERCA ( Fig. 5A, B), ER Ca 2+ ( Fig. 5D, E) 수준과 MMP ( Fig. 5F, G)의 경우 유의하게 감소하여 ( p =.001), ER 스트레스가 발생하였음을 확인하였다. 그러나 palmitate에 의해 ER 스트레스가 야기된 조골세포에 근수축에 의해 방출된 EVs 처치그룹인 EP 의 경우 PAL에 비해 모두 유의하게 개선되는 효과를 확인하였다( Fig. 5A- G). 이러한 결과는 골격근 수축으로 방출된 EVs는 조골세포에 작용하여 palmitate로 야기된 ER 스트레스를 개선한다는 것을 알 수 있다.
Fig. 5.
Fig. 5.ER stress induced by palmitate leads to bone loss, but skeletal muscle contraction improves this condition. When osteoblasts are treated with palmitate for 12 hours, ER stress increases (A-C), ER Ca2+ levels decrease (D, E), and MMP also decreases (F, G). However, treating cells with extracellular vesicles (EVs) released through skeletal muscle contraction in cells experiencing osteoblast ER stress improves bone loss through the NFκB and RANKL-OPG pathway related to bone loss (H-L). CON, control group; EV, extracellular vehicles treated group; PAL, palmitate treated group; EP, extracellular vehicles+palmitate treated group. * p<.05, ** p<.05, *** p<.001. 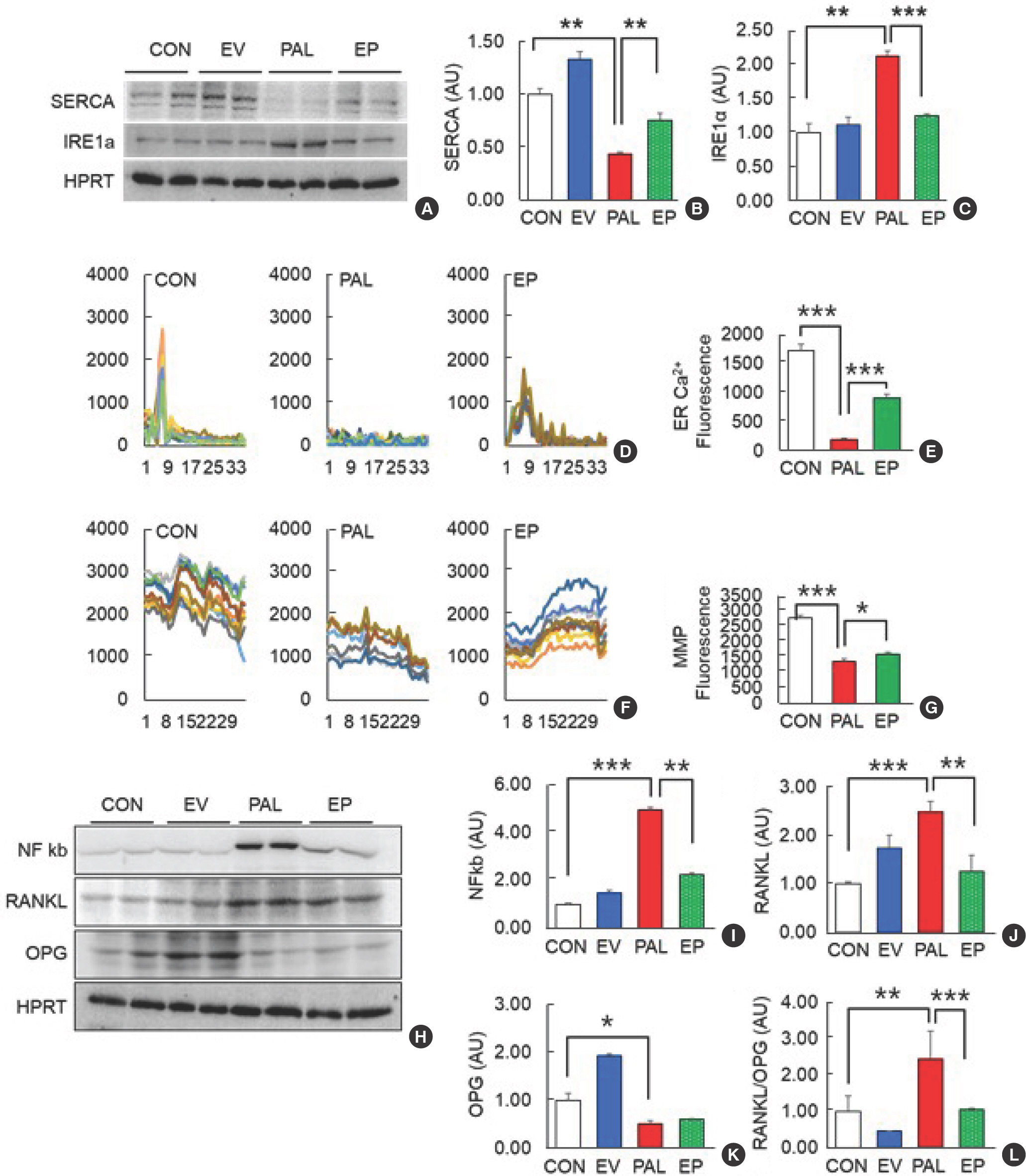
이에 본 연구는 추가적으로 골격근 수축에 의해 방출된 EVs가 ER 스트레스에 의해 유도된 골 손실 환경을 개선하는가를 분석하였다. PAL은 CON에 비해 NFκB ( Fig. 5H, I), RANKL ( Fig. 5H, J), 그리고 RANKL/OPG ratio ( Fig. 5L)가 유의하게( p <.01) 높았으며, OPG ( Fig. 5H, K)는 유의하게( p <.05) 낮았다. 이는 palmitate에 의해 골 손실 관련 기전이 향상됨을 의미하는데, EV의 경우 PAL에 비해 OPG는 차이가 없었으나, NFκB ( Fig. 5H, I), RANKL ( Fig. 5H, J), 그리고 RANKL/OPG ratio ( Fig. 5L)를 유의하게( p<.01) 개선하였다.
논 의
본 연구는 조골세포에 ER 스트레스를 유도하여 골 손실 환경을 유도한 후 중력 또는 체중부하에 따른 효과를 배제한 상황에서 골격근 수축으로만 활성화된 골 손실 관련 기전의 개선에 따른 골 손실 환경을 개선하는가를 분석하고자 하였다. 이를 위한 선결과제는 조골세포 ER 스트레스를 유도하여 골 손실 환경이 이루어지는가를 확인하는 것이다. Palmitate와 같은 포화지방산의 체내 축적은 체내 지질 독성을 축적하여 ER 스트레스를 야기함으로써 세포기능을 저해하는데[ 14], 본 연구( Figs. 2, 3) 또한 palmitate에 의해 조골세포 ER 스트레스가 유도되었다. 인간의 골수세포에 palmitate를 처치할 경우 ER 스트레스 관련 인자인 IRE1α 등의 발현이 증가한다[ 15]. 세포 내 낮은 수준의 Ca 2+의 농도는 ER에서의 Ca 2+ pump와 inositol triphosphate receptor (IP3R) 또는 ryanodine receptor (RyRs)에 의해 세포질 외 공간으로 방출되는데[ 16, 17], 이러한 과정에서 SERCA에 의해 ER로 재흡수 되게 된다[ 18]. 그러나 ER 스트레스는 본 연구의 Fig. 2C와 같이 SERCA의 발현이 감소되기 때문에 Ca 2+의 재흡수는 방해받게 되고 결국 Fig. 2D- F처럼 거의 고갈 수준에 이르게 된다. 뿐만 아니라 ER 스트레스로 인한 Ca 2+의 고갈은 미토콘드리아 기능을 조절하는데, succinate dehydrogenase와 같은 미토콘드리아 효소가 Ca 2+ pool에 의해 민감하게 반응하기 때문이다. 만약 Ca 2+이 감소하게 되면 미토콘드리아 효소의 활성이 감소하여 미토콘드리아에 의한 에너지 생성은 감소되는데[ 19], 이러한 과정에서 미토콘드리아 막 전압은 감소하여 그 기능은 저하된다[ 20, 21]. 이러한 결과는 본 연구의 Fig. 2G- I와 동일한 결과이다. 또한 골수에 유래된 대식세포에 SERCA를 억제할 경우 ER 스트레스 유발과 함께 RANKL 발현과 osteoclast 과잉 합성으로 골손실이 유도될 뿐 아니라[ 22] palmitate 에 의한 ER 스트레스 또한 조골세포에서 NFκB signiling을 통해 골 손실을 유도한다[ 23]. 즉, 이러한 연구는 Fig. 3처럼 palmitate에 의한 ER 스트레스가 NFκB와 RANKL/RANK/OPG pathway를 통해 골 손실이 유도된다는 것을 알 수 있다. Palmitate 처치에 따른 조골세포 ER 스트레스에 의한 골 손실 환경을 개선하기 위한 근수축 효과를 검증하기 위해 뼈와 근육이 상호작용하는가를 분석하였다. 골격근 세포의 지속적인 수축은 세포 항상성의 증가 및 대사질환에 효과적으로 대처할 수 있는 적응 현상을 유도한다[ 24]. 이를 위해 골격근 수축 시 운동유발 물질이 exosome에 둘러싸여 방출된다[ 25]. 특히 HSP70, CD63, αB-crystallin 등이 특이적으로 exosome에 포함되어 세포 간의 소통을 조절 또는 세포를 보호하는 역할하기 때문에 흔히 exosome marker로 사용된다[ 26, 27]. 본 연구 또한 골격근 세포를 전기 자극하여 근수축을 유도한 결과 Fig. 4A, B처럼 exosome 특이 단백질인 HSP70과 αB-crystallin이 추출된 exosome에서 확인되었으며, 비 특이 단백질인 calnexin은 확인할 수 없었다. 즉 이는 전기자극에 의한 골격근 수축은 exosome을 통해 운동유발물질이 전달됨을 의미한다. 이에 골격근의 수축에 의해 분비되는 exosome이 뼈에 작용하는가를 알아보기 위해 CD63-eGFP Plasmid DNA를 골격근세포에 transfection한 후 전기 자극하여 방출된 exosome을 다시 조골세포에 처치하였으며, 형광 현미경을 이용하여 조골세포에서의 GFP 발현 유 · 무를 관찰하였다. 그 결과 Fig. 4C처럼 골격근에 transfection 한 CD63-GFP 단백질이 조골세포에서 확인되었다. 이는 골격근 수축에 따른 운동유발물질이 exosome을 통해 뼈에 작용할 수 있음을 의미하는데, 본 연구의 Fig. 5는 이러한 주장을 뒷받침한다. 앞서 Figs. 2, 3에서 살펴본 것처럼 palmitate에 의해 유도된 조골세포 ER 스트레스에 의해 유발된 골 손실 관련 기전의 활성에 따른 골 손실 환경은 근수축에 의해 방출된 exosome에 의해 개선되었다. 즉, ER 스트레스에 의한 골 손실의 경우 근수축에 의해 ER 스트레스 감소, SERCA에 의한 Ca 2+ 재흡수 증가, 미토콘드리아 기능 향상, 그리고 RANKL/RANK/OPG pathway에 의한 골 손실 관련 기전이 개선됨을 알 수 있다.
결 론
Palmitate는 ER Ca2+을 감소시키고, 조골세포 ER 스트레스를 유발함과 동시에 미토콘드리아 기능도 저하시킨다. 뿐만 아니라 골 손실 관련 핵심 기전인 RANKL/RANK/OPG pathway를 통해 골 손실 환경을 유도하지만, 근수축작용에 따른 운동유발 물질은 exosome을 통해 조골세포에 작용하여 이를 개선할 수 있다. 따라서 기존의 웨이트 트레이닝과 줄넘기 등의 체중 부하 운동뿐 아니라 체중 부하가 심하지 않은 형태의 근수축 운동 또한 골 손실을 예방할 수 있을 것이다. 또한 이러한 결과는 다양한 건강상의 문제로 인해 신체활동이 불가능한 사람을 위한 운동방법 및 운동약물 등을 개발하는데 도움이 될 것이다. 그렇지만 본 연구는 세포를 이용한 연구로서 palmitate에 의한 직접적인 골 손실은 확인하지는 못하였다. 이에 좀 더 명확한 결론을 위해서는 동물실험 등을 통한 추가연구가 필요할 것이다.
REFERENCES
1. Qiao D, Li Y, Liu X, Zhang X, Qian X, et al. Association of obesity with bone mineral density and osteoporosis in adults: a systematic re-view and meta-analysis. Public Health. 2020;180:22-8.   6. Min SK, Oh T, Kim SH, Cho J, Chung HY, et al. Position statement: exercise guidelines to increase peak bone mass in adolescents. Exercise Science. 2020;29(1):10-23.   7. Kang YS, Kim JC, Kim JS, Kim SH. Effects of swimming exercise on serum irisin and bone FNDC5 in rat models of high-fat diet-induced osteoporosis. J Sports Sci Med. 2019;18(4):596.   8. Hart K, Shaw J, Vajda E, Hegsted M, Miller S. Swim-trained rats have greater bone mass, density, strength, and dynamics. J Appl Physiol. 2001;91(4):1663-8.   9. Falcai MJ, Zamarioli A, Okubo R, de Paula F, Volpon JB. The osteo-genic effects of swimming, jumping, and vibration on the protection of bone quality from disuse bone loss. Scand J Med Sci Sports. 2015;25(3):390-7.   10. Kawanishi N, Tominaga T, Suzuki K. Electrical pulse stimulation-in-duced muscle contraction alters the microRNA and mRNA profiles of circulating extracellular vesicles in mice. Am J Physiol Regul Integr Comp Physiol. 2023;324(6):R761-R71.   18. Periasamy M, Kalyanasundaram A. SERCA pump isoforms: their role in calcium transport and disease. Muscle Nerve. 2007;35(4):430-42.   19. Panov AV, Scaduto RC. Influence of calcium on NADH and succinate oxidation by rat heart submitochondrial particles. Arch Biochem Biophys. 1995;316(2):815-20.   23. Zhong X, Xiu L, Wei G, Pan T, Liu Y, et al. Bezafibrate prevents palmitate-induced apoptosis in osteoblastic MC3T3-E1 cells through the NF-κB signaling pathway. Int J Mol Med. 2011;28(4):535-42.  26. Lawson C, Vicencio JM, Yellon DM, Davidson SM. Microvesicles and exosomes: new players in metabolic and cardiovascular disease. J En-docrinol. 2016;228(2):R57-R71.   27. Bakthisaran R, Tangirala R, Rao CM. Small heat shock proteins: role in cellular functions and pathology. Biochim Biophys Acta Proteins Proteom. 2015;1854(4):291-319.  
|
|










