트레드밀 운동이 자폐스펙트럼장애 모델 마우스의 자폐행동 및 전두엽 피질 SHANK 수용체에 미치는 영향
Abstract
PURPOSE
The first aim of this study is to change autistic behavior in Shank3B Knock-Out (KO) mice through treadmill exercise (TD), and the second aim is to alter SHANK protein receptors in the prefrontal cortex (PFC) of mice through TD.
METHODS
Male mice were divided into Control (11-week-old, n=8), Control+TD (n=8), Shank3B KO (n=8), and Shank3B KO+TD (n=8). Control and Shank3B KO mice were exercised using TD for 2 weeks for 30 minutes each to observe the effects of exercise.
RESULTS
Compared to the control group (C57BL/6J), Shank3B KO mice showed excessive self-grooming behavior; however, TD reduced repetitive behavior (p<.05). The effect of TD was also seen in the behavior of Shank3B KO mice evaluated by measuring social interaction time using the two-chamber social behavior test and socio-sexual behavior test (p<.05 compared to control). Differences were found in C57BL/6J and Shank3B KO mice by assessing proteins such as GluR2, Homer1, phosphorylated GSK-3α/β, and phosphorylated Akt1 in the PFC. The results suggested that TD yielded better outcomes in Shank3B KO+TD mice than in Shank3B KO mice.
CONCLUSIONS
TD positively affected behavioral changes in repetitive behavior and social interaction defects in autism spectrum disorder (ASD) model mice. Alterations were also observed in the SHANK glutamate receptor and SHANK sub-signal transporter phosphorylation protein. This suggests that TD is an effective way to improve autistic behavior in ASD. However, further research is necessary to clarify the effects of TD by studying the underlying mechanisms and changes in SHANK proteins and other factors.
Keywords: Shank3B, Knock-Out (KO), Repetitive behavior, Social interaction, Glutamate receptor
색인어: Shank3B, Knock-Out (KO), 반복적인 행동, 사회적 상호작용, 글루타메이트 수용체
서 론
자폐스펙트럼장애(Autism Spectrum Disorder, ASD)란 사회적 의사소통 및 상호작용의 행동 이상과 고정관념적인 반복 행동을 포함하는 신경발달장애(Neurodevelopmental Disorder)이다[ 1]. 자폐스펙트럼장애는 생애 초기에 발병되는 뇌 발달과 뇌 신경 구성으로 인해 발생을 하며[ 2], 자폐성 장애와 아스퍼거 장애 및 달리 명시되지 않은 전반적 발달 장애(PDD-NOS)로 구분된다[ 3]. 대뇌 피질의 신경 회로가 정상적인 성장 패턴보다 미숙하게 발달되어 대뇌 피질 영역 간의 연결이 부족해져 언어, 사회적 상호작용 결함 및 행동 결함의 증상들이 보이게 된다[ 4]. 자폐증은 초기에 발병되는 질병이므로 초등학교 이후, 청소년 또는 자폐스펙트럼장애 증상을 보이는 가족이 있는 성인의 경우에는 불안과 과잉행동 또는 심적 변화 장애와 같은 문제가 동시 다발적으로 발생하는 경우가 많다[ 5]. 자폐스펙트럼장애는 발병은 초기 발달과정의 가설 이외에도, 아동이나 청소년 및 가정환경에 부정적인 영향을 미칠 수 있는 신체적 정신적, 신경 발달 및 기능적 질환 등 수많은 질환과 밀접한 관련이 있다[ 6]. 자폐스펙트럼장애의 치료제로 사용 중인 항우울제-SSRI (Selective Serotonin Reuptake Inhibitor), 항정신병 약물, 항경련제, 각성제 등 많은 치료가 나와있으나, 자폐스펙트럼장애 증상을 치료하는데 있어 체중증가, 대사증후군, 빈맥 등 다양한 부작용들을 동반하고 있다[ 7]. 이러한 부작용들로 인하여 비약물적인 치료 방법 중 하나인 운동은 신체 활동으로 인한 자폐스펙트럼장애와 같은 신경발달장애의 비정상적인 행동에 대한 잠재적인 치료 방법으로 여겨지고 있다[ 8, 9]. 인간 대상으로 연구를 실행한 비약물적인 치료법으로 부모-자녀 간의 상호작용 치료 중 하나인 수동 치료법은 아동에게서 정서와 적응성을 긍정적으로 증가시켰으며[ 10], 부모 교육만 실시한 것보다 자녀와 같이 교육을 실시하였을 때, 공격적인 행동을 더 감소시킨다는 결과를 보여주었다[ 11]. 또 다른 연구에서 자폐스펙트럼장애가 있는 남자 아이 16명 대상으로 수중 수영 운동(Water Exercise Swimming Program, WESP)을 20주간 실시 후 사회적 결함 행동에 대한 긍정적인 결과를 보여주었다[ 8]. Silk et al. [ 12], Horwitz et al. [ 13], Sears et al. [ 14]의 자폐스펙트럼장애 환자를 대상으로 한 연구에 의하면, 자폐스펙트럼장애가 있는 사람에 대한 기능적 자기 공명 영상(fMRI) 분석 결과, 전두엽 피질, 특히 실행 기능에 결정적으로 관여하는 영역인 전대상회(Anteri-or Cingulate Cortex, ACC)의 분할에서 대사적 감소를 나타내었다. 이 지역은 측면 전두엽 피질 및 후두정엽 피질에 연결되어 있어, 공간 방향 및 기억과 관련된 감각 기능과 공간감각 인식에 이상이 있음을 간접적으로 나타낸다. Shank3 유전자의 반수체부족성(Haploinsufficiency)은 인간 유전학 연구에서 자폐증과 관련이 많은 것으로 알려져 있으며[ 15], Shank3 유전자는 인간 염색체 22q 13.3 결손(delection)에 의해 생기는 Pelan-Mc-dermid Syndrome (PMDS)의 원인으로 알려져있다[ 16]. PMDS는 신경발달 장애로 전반적인 발달 장애와 지적 장애, 운동 기능 저하, 자폐스펙트럼장애를 기반으로 하며, PMDS에서 자폐스펙트럼장애 유병률이 약 94%의 비율을 차지하고 있다고 알려져있다[ 16]. SHANK의 손상으로 인해 신체의 기능과 신경계에 영향을 미치고 있으며, 인간의 신체 발달 지연은 생후 첫 12개월 동안 그 증상을 보인다[ 17]. 신호 전달 경로에서 단백질 상호작용을 제어하고, 세포질 신호 전달에 관여하며, 단백질의 상호 작용을 조절하는 기능을 하는 SRC 상동성3 (SH3)와 다중 안키린 도메인 단백질(SHANK)은 SHANK1, SHANK2, SHANK3 유전자에 의해 발현된다[ 18]. 세 가지 다른 SHANK 유전자는 발달 단계, 세포 유형 및 뇌 영역에 따라 차등적으로 발현되는 여러 단백질을 생성할 수 있으며, SHANK 유전자 중 신경정신질환 사이의 연관성이 많은 것은 Shank3 유전자이다[ 18]. Shank3의 행동학적 특징으로 자폐적 행동과 사회적 행동 장애가 공통적으로 보여지며, Shank3 결실이 시냅스 후 밀도(Postsynaptic protein domain, PSD)에서 단백질 구성을 방해하고 신경 전달 효율을 감소시켜 자폐증과 같은 행동을 보여준다[ 19, 20]. 자폐스펙트럼장애의 증상 중 하나인 반복적인 행동은 자폐증 환자와 자폐스펙트럼장애 모델 마우스에서 나타나는데, 그중 Shank3와 상호 작용하고 선조체에서 발현되는 SAPAP3의 결함 마우스에서 피질-선조체 회로 기능 장애 및 반복적인 행동과 강박적인 그루밍을 포함하는 강박장애(Obsessive-compulsive disorder, OCD)유사 행동을 보여준다[ 4]. Shank3는 시냅스 후 밀도 분자 신호 전달 복합체이며[ 21, 22], 시냅스 발달, 기능 및 가소성을 조절하는 시냅스 후 스캐폴딩 단백질이다[ 23]. PSD95-SAPAP-SHANK 단백질은 뉴로렉신-뉴로리긴 복합체를 포함하는 시냅스 단백질과 상호작용하는 글루타메이트성 시냅스에서 시냅스 후 스캐폴드를 형성한다[ 23]. 이후 시냅스에서 GKAP, HOMER 구조단백질, AMPA, NMDA 글루타메이트 수용체의 발현 감소와 더불어 흥분성 시냅스의 기능적 약화가 연구되었다[ 24]. 신경 발달과 인지 기능의 배경이 되는 시냅스의 기능을 제어하는 PSD 단백질인 NMDA 글루타메이트 수용체는 Shank3와 연관성이 있으며, 시냅스와 관련있는 글루타메이트 수용체 서브 유닛 중 하나인 GluR2는 Homer와 결합하여 SHANK 유전자에 영향을 끼치는 것으로 알려져있다[ 25]. Shank3는 중추신경계의 발달과 기능에 중요한 역할을 하는 유전자로, 트레드밀 운동과 같은 외부요인으로 간단하게 발현될 수 있는 요인은 아니다. 하지만, 운동은 뇌에서 새로운 시냅스를 형성하고 기존의 시냅스를 강화하는 것으로 알려져있다[ 26]. 선행 연구에서 전두엽 피질(Prefrontal cortex, PFC)은 인간과 동물 모델에서 비정상적인 흥분성 회로와 다양한 연결성을 나타내었다[ 27]. 중추신경계 회로의 결함이 Shank3B KO 마우스의 감각 이상에 많은 영향을 미친다는 것을 보여주었으며, Shank3B KO 마우스의 초기 발달 과정에서 피질-선조체 상호 작용 사이의 비정상적인 상호작용과 같은 결함이 나타났다[ 28]. 뉴런의 수상돌기 성장에 관여하는 GSK-3β는 MAPK 신호와 같은 많은 세포골격 단백질을 인산화하며 수상돌기 발달을 조절한다[ 29]. GSK-3β와 SHANK3의 시냅스와 상관관계가 있는 주요 AMPA 수용체인 글루타메이트 수용체 2 (GluR2)의 발현이 Shank3B KO 마우스에서 크게 감소하였다. 또한 GSK-3β 활성을 조절하는 단백질 중 Akt는 Shank3B KO 마우스에서 증가하는 경향을 보였다[ 28]. 이러한 결과로 보았을 때, Shank3B KO 마우스에서 글루타메이트 수용체에 관련된 GSK-3β와 Akt는 자폐스펙트럼장애에 관련되어 있음을 시사한다. 따라서 본 연구의 목적은 자폐스펙트럼장애의 행동학적 변화 예방과 치료적 접근을 위한 요인으로서 자폐스펙트럼장애 모델 Shank3B KO 마우스에서 트레드밀 운동으로 인한 행동학적 변화와 전두엽 피질 SHANK 수용체 관련 단백질인 GluR2, Homer1, p-PSD95, p-Akt1, p-GSK-3α/β의 변화를 규명하고자 한다.
연구 방법
1. 연구 대상
1) 실험 동물
본 실험에 사용한 실험 동물은 C57BL/6J 마우스(n=16)와 B6.129-Shank3<tm2Gfng/J> (JAX 174; Labatory, USA)를 사용했으며, 1964년 발표한 헬싱키 선언의 Guiding Principles for the care and Use of Ani-mal에 따라 온도(23°C), 습도(40-60%) 및 주간(06:00-18:00)에 점등(18:00-06:00)에 자동적으로 소등되는 시설을 갖춘 K대학교 동물실험실에서 사육하였다. 실험기간 동안 미국영양학회에서 발표된 실험동물용 식이 조정에 따라 제조된 사료(SAFE 40+RMM 쥐사료 – 3230)를 제공하고 식이와 수분섭취는 제한 없이 공급하였다. 실험집단은 대조군 집단(male, n=8), 대조군+트레드밀 운동 집단(male, n=8), Shank3B KO 집단(male, n=8), Shank3B KO+트레드밀 운동 집단(male, n=8)으로 구분하였으며, 모든 실험 절차 진행은 K대학교 동물실험윤리위원회의 승인을 받아 진행하였다(IACUC-2022-08).
2) 자폐스펙트럼장애 마우스 모델 확립
본 실험에 사용한 실험동물 B6.129-Shank3<tm2Gfng/J> (Shank3B KO)은 Jackson 실험실(JAX 174; Labatory, USA)에서 분양 받았으며, Shank3B +/- 마우스와 Shank3B +/- 마우스를 교배시킨 뒤 11주령 된 Shank3B KO (-/-) 수컷 마우스를 사용하여 실험을 진행하였다. 교배한 후 모델 확인하기 위해 Jackson 실험실(JAX; Labatory, USA)에서 사용되는 Common 프라이머(GAGACTGATCAGCGCAGTTG), Wild type Reverse 프라이머(TGACATAATCGCTGGCAAAG), Mutant Reverse 프라이머(GCTATACGAAGTTATGTCGACTAGG)를 사용하였다. 마우스 1마리당 2× Immomix Red를 10 µ L, Common 프라이머 0.3 µ L, Wild type Reverse 프라이머 0.3 µ L, Mutant Reverse 프라이머 0.3 µ L와 H2O 8.1 µ L씩 넣고 혼합한 뒤, T100 Thermal Cycler (Bio-Rad Laboratories, USA)에 넣어 94°C 10분, 94°C 15초, 65°C 15초, 68°C 15초(10번 반복, −0.5°C씩 감소), 94° C 15초, 60°C 15초, 72°C 30초(20번 반복), 72°C 10분, 10°C 유지 상태 과정을 끝낸 후 DNA를 1 µ L, Dyne Loading star 2 µ L씩 혼합한 뒤, 1.5% Gel Agarose in 1x TAE에 Dyne 100bp DAN Ladder(Dyne Loading Star mixed) 3 µ L씩 주입 후 DNA를 5 µ L씩 주입하여 100 V, 28 min 전기영동하였다. 이미지 분석 시스템(Molecular Imager ChemiDoc XRS System, Bio-Rad, USA)을 이용하여 스캔한 과정을 다 마쳐 마우스를 분리한 후 11주령에 맞춰 실험에 사용하였다.
2. 연구절차
1) 운동 처치
본 실험은 C57BL/6J (대조군) 마우스와 Shank3B Knock-Out (KO) 마우스를 대상으로 동물용 트레드밀(B.S Technolab INC., Seoul, Korea)에서 경사도를 0%로 고정시킨 후에 하루 30분씩 주 5일, 2주간 실시하였다. 경사도를 0%로 고정시킨 후에 중강도 부하의 강도로 실시하였다(운동시작 30분; 6-10 m/min). 이 연구에서 활용한 운동 프로토콜은 Sigoli et al. [ 30]이 제시한 중강도 운동 프로그램을 수정하여 실시하였다. 운동 프로토콜은 다음 Table 1과 같다.
Table 1.
Treadmill exercise protocol
|
Intensity |
Time |
Gradient (%) |
Frequency (day) |
|
6-10m/min |
30 min |
0 |
5 |
2) 자폐행동 검사
Self-grooming behavior test (홈케이지)를 통해 Shank3B KO 마우스의 행동학적 특징 중 하나인 반복적인 행동을 검사하였다. 마우스를 홈케이지에 넣고 10분 적응시킨 뒤 이후 10분을 측정하였으며, 10분 동안 머리, 얼굴, 귀, 몸통을 핥거나 문지르는 행동 시간을 측정하였다. Self-grooming duration (sec)과 self-grooming count(rep)을 측정하였으며, 그루밍 행동이 3초 동안 지속 시 한 번의 횟수로 나타내고 그루밍 행동이 3초 동안 멈추었을 시 다시 횟수를 세었다. Two-chamber social behavior test (SMART; Panlab S.I., Barcelona, Spain)를 Smart video tracking software (smart v3.0 program)를 통하여 마우스의 행동을 검사하였다. 중간 통로(가로 8 cm×세로 10 cm x 높이 26 cm)로 분리된 양측 필드(가로 26 cm×세로 26 cm)에 빈 원형 그리드 케이지(지름 12 cm×높이 33 cm) 속으로 표적 마우스 C57BL/6J를 넣어 실험용 타겟 마우스를 3분 적응시킨 뒤 빈 원형 그리드 케이지에 표적 마우스 C57BL/6J를 넣어 1분 적응, 이후 5분을 측정하였으며, 마우스 간의 상호 스니핑 시간을 분석하였다. Socio-sexual behavior test (SMART; Panlab S.I., Barcelona, Spain)를 Smart video tracking software (smart v3.0 program)를 통하여 마우스의 행동을 분석하였으며, 성별에 따른 사회적 상호작용 결함을 검사하였다. 사각형 필드(45 cm×45 cm×40 cm)에 수컷 마우스와 C57BL/6J 암컷 표적 마우스를 넣어 10분을 측정하였으며, 코와 코 스니핑 시간과, 항문 스니핑 행동 시간을 분석하였다.
3) 조직 적출
실험동물을 주 5일, 2주간 동물용 트레드밀 운동시킨 후 자폐행동 검사를 수행하고, 럼푼(바이엘코리아 주식회사, Korea)과 졸레틸50 (Virbac, France)을 혼합하여 80 mg/kg을 복강 내 주입시켜 마취시킨 후, 뇌 조직을 지역별로 적출하여 분석 시까지 −80℃ 초저온냉동고(Deep Freezer, SANYO, Japan)에서 보관하였다.
4) SDS-PAGE
10-12% separating gel (30% acrylamide:bis-acrylamide, 1.5M tris pH 8.8, 10% SDS, TEMED, 10% ammonium persulfate)과 5% stacking gel (30% acrylamide:bis-acrylamide, 1M tris pH 6.8, 10% SDS, TEMED, 10% ammonium persulfate)을 사용하였다. 원심분리(15,000 rpm, 15분)한 상층액과 SDS loading buffer (2% SDS, 14.4 mM 2-mercaptoethanol, 0.1% Bromophenol blue, 60 mM tris pH6.8, 25% glycerol)를 혼합한 후 70℃에서 10분간 끓여 단백질을 변성시킨 후 식혀서 다시 15,000 rpm으로 15분간, 4℃에서 원심분리하고 standard 마커(SDS-PAGE Molecular Weight Standards, Bio-Rad)로 각 sample을 Mini-ProteinⅡ dual-slab apparatus (Bio-Rad)에 준비된 Stacking gel well에 단백질량이 10 µ g이 되도록 분주하고 100 Volt에서 1시간 30분 정도 샘플이 바닥에 닿을 때까지 전기영동하였다.
5) Western blot analysis
Nitrocellulose Blotting membrane을 MeOH에 적셔 활성화시킨 후에 Transfer buffer (0.05% SDS, 20% methanol, 190 mM glycine, 50 mM Tris-base)로 washing한 후에 Transfer buffer에 적신 whatman 3M paper를 차례로 겹쳐 Mini trans-bolt cell (Bio-Rad, CA, USA)에 장치한 후 200mA로 60분 전사하고 Membrane으로 증착이 끝나면 rocker platform 위에서 60분 동안 membrane을 각 5% Skim milk (in TBS-T: 150 mM NaCl, 0.05% Tween-20, 10 mM tris-base pH 7.4), 5% BSA(in TBS-T: 150 mM NaCl, 0.05% Tween-20, 10 mM tris-base pH 7.4)로 Blocking 시켰다. 1차 항체 Glutamate receptor 2 Polyclonal antibody (#11994-1-AP, proteintech, USA), Anti-Hom-er1 antibody (#ab184955, abcam, England), Anti-PSD95 (phospho T19, EPR2619(2), abcam, England), Anti-GSK-3α/β (phospho Ser21/9, #9331, Cell Signaling, USA), Anti-Akt1 (phospho 5.Ser 473, sc-293125, Santa Cruz Biotechnology, Europe), Anti-GAPDH (6C5, sc-32233, Santa Cruz Biotechnology, Europe), Anti-β-actin (sc-47778, Santa Cruz Biotechnology, Europe)는 1: 1000으로 각 5% Skim milk (in TBS-T: 150 mM NaCl, 0.05% Tween-20, 10 mM tris-base pH 7.4), 5% BSA (in TBS-T: 150 mM NaCl, 0.05% Tween-20, 10 mM tris-base pH 7.4) 용액에 각각 희석시켜 4°C, 8시간 동안 반응시킨 다음 TBS-T 용액으로 10분 씩 3차례 세척한 후 2차 항체(horseradish per-oxidase-Conjugated goat anti-rabbit, CA, USA; horseradish peroxidase-Conjugated goat anti-mouse, CA, USA) 를 Blocking 용액으로 1: 2,000으로 희석시켜 2시간 동안 반응시킨 다음 TBS-T 용액으로 10분씩 3차례 헹구고 마지막 단계로 Western Blotting Luminol Reagent (WBLR) solution에 membrane을 넣고 2분간 반응하였다. Membrane을 이미지 분석 시스템(Molecular Imager ChemiDoc XRS System, Bio-Rad, USA)을 이용하여 스캔한 후 Quantity One 1-D Analysis Software (Bio-Rad, USA)를 이용하여 단백질량을 산출하였다.
3. 자료처리방법
이 연구에서 얻어지는 모든 자료는 GraphPad Prism 8 통계 프로그램을 이용하여 기술통계치(Mean±SD)를 산출하였다. 각 집단 간 변인의 차이를 확인하기 위해서 일원변량분석(One way ANOVA)을 실시하였으며, 집단 간 유의한 차이가 있을 경우 Bonferroni (least significant difference) 방법을 이용하여 사후 검증을 실시하였다. 모든 검증에 통계적인 유의수준은 α=0.05로 설정하였다.
연구 결과
1. 자폐스펙트럼장애 동물 모델인 Shank3B KO 마우스 자폐 행동
본 연구에서 동물용 트레드밀 운동을 시작하기 전에 마우스 모델링을 확인하기 위해 Genotyping을 실시하였으며, C57BL/6J 마우스와 Shank3B KO 마우스를 Genotyping을 통해서 밴드의 위치로 유전자 분석을 하였으며( Fig. 1A), 대조군 집단인 C57BL/6J 모델 마우스와 KO 집단인 Shank3B KO 모델 마우스를 분리하였다. 반복적인 행동인 그루밍으로 인해 털 빠짐 모습은 대조군 집단과 Shank3B KO 마우스의 차이를 비교할 수 있으며( Fig. 1B), 모델링 확인 후 실험 진행을 하였다( Fig. 1C).
Fig. 1.
Fig. 1.Genetically modified ASD (Shank3B-/-) model. (A) PCR-based detection of wild-type and Shank3B gene knock-out, (B) Shank3B KO mice dis-playing skin-lesion, (C) Experimental design. 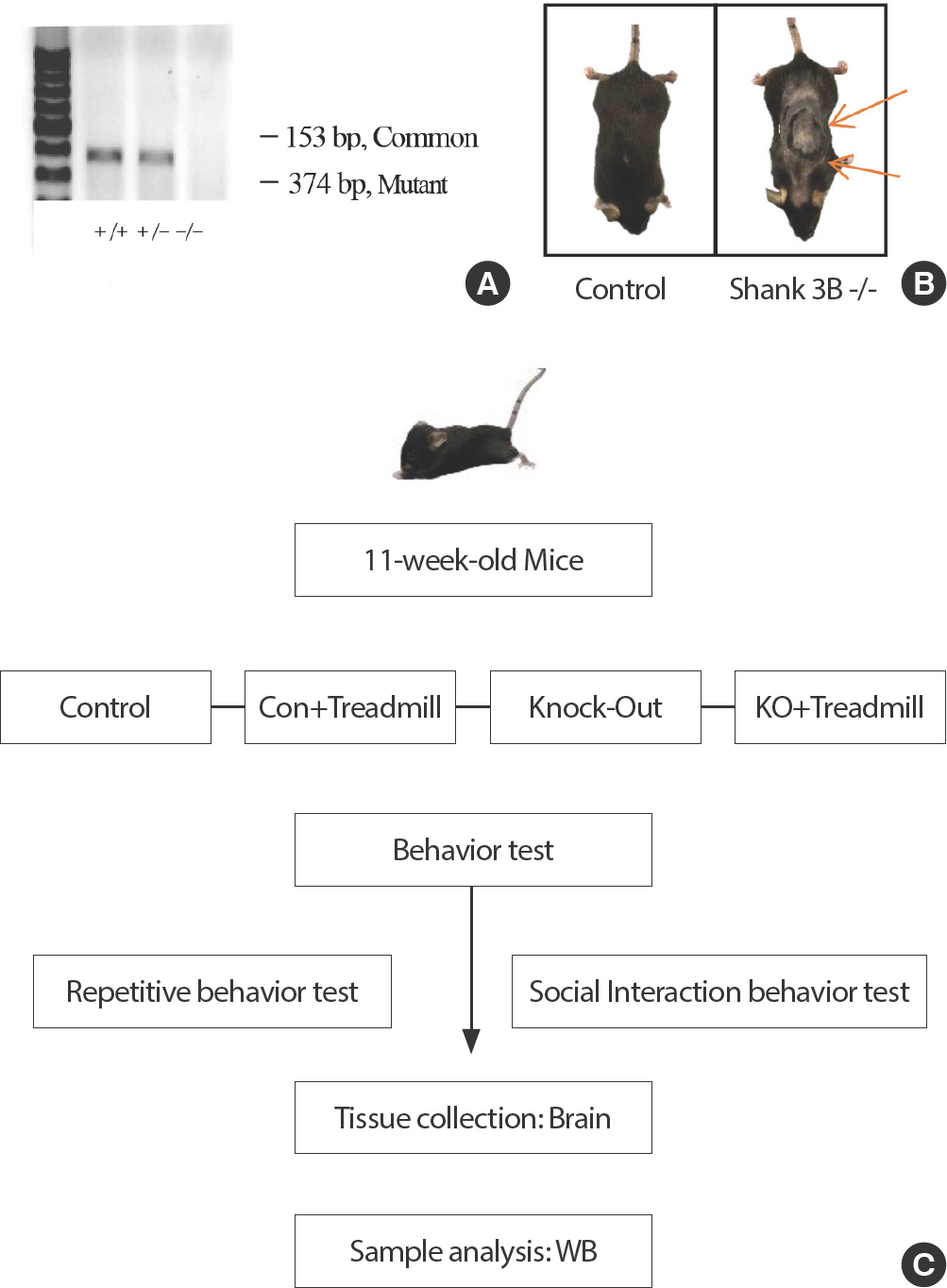
2. 트레드밀 운동 처치로 인한 반복적인 행동 변화
본 연구에 C57BL/6J (WT) 마우스와 Shank3B KO (KO) 마우스를 대상으로 동물용 트레드밀(B.S Technolab INC., Seoul, Korea)을 이용하여 주 5일, 2주 동안 6-10 m/min 중강도로 실시하였으며, 동물용 트레드밀 운동 실행 후 C57BL/6J 마우스와 Shank3B KO 마우스의 반복적인 행동인 Self-Grooming behavior 실험을 하였으며, 홈케이지에서 실험을 진행하였다. Self-grooming duration (sec)과 Self-grooming duration (rep)에 대해 통계적 검증을 실시한 결과( Fig. 2A), Self-grooming count (rep)에서 대조군 집단에 비해 Shank3B KO 집단이 유의미하게 증가하였으며( p<.001), Shank3B KO 집단과 Shank3B KO+트레드밀 운동 집단의 Self-grooming duration (sec)에서 유의미하게 감소되는 것으로 나타났다( p <.001). 그루밍 행동이 3초 동안 지속이 되면 1번의 횟수가 올라가는 grooming count (rep)에서는 대조군 집단과 Shank3B KO 집단, Shank3B KO+트레드밀 운동 집단 간의 유의한 차이가 나지 않았다.
Fig. 2.
Fig. 2.Exercise-induced significant improvement of autistic behavior in ASD model (A) The self-grooming duration and count in grooming behavior test. * p<.05, Bonferroni post hoc test after ANOVA. All values are expressed in the means±SD. *** p<.001 versus KO Group; ### p<.001 versus KO Group. 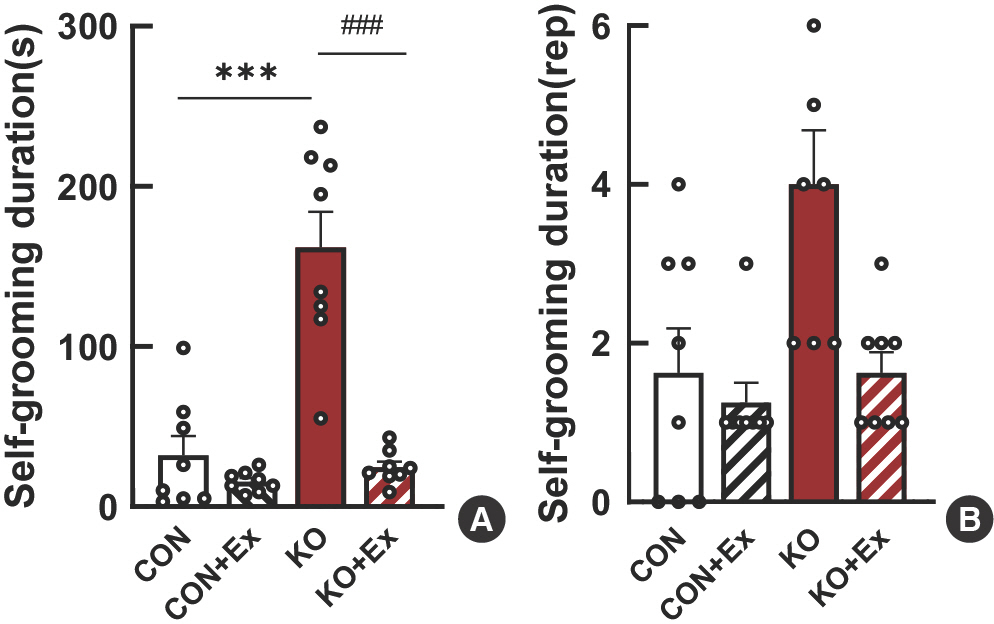
3. 트레드밀 운동 처치로 인한 사회적 상호작용 행동 변화
사회적 상호작용 결함을 보여주는 Two-chamber social behavior test를 진행하였으며, 표적 마우스 암컷을 사용하여, 대조군 집단과 대조군+트레드밀 운동 집단, Shank3B KO 집단, Shank3B KO+트레드밀 운동 집단으로 실험하였으며, 표적 마우스가 들어있는 챔버 안에 암컷 마우스가 들어있는 원통 케이지에 대한 스니핑 행동에서는 대조군 집단에 비해 Shank3B KO 집단의 Time spent sniffing (sec)이 유의미하게 감소하였으며( p<.001), Shank3B KO 집단에 비해 Shank3B KO+트레드밀 운동 집단에서 유의미하게 증가하는 것을 확인하였다( p <.05) ( Fig. 3A). Socio-sexual behavior test는 수컷-암컷의 Sexual social interaction을 보기 위한 실험으로 알려져 있으며, 운동 처치의 효과를 확인하였다. 대조군 집단에 비해 Shank3B KO 집단의 Time spent nose-nose sniffing (sec)이 감소하였으며( p<.05), Shank3B KO에 비해 Shank3B KO+트레드밀 운동 집단에서 유의미하게 증가하는 것을 확인하였다( p <.001). Time spent anus sniffing (sec)에서 역시 대조군 집단과 Shank3B KO 집단에서 유의한 차이를 보였으며( p <.001), Shank3B KO+트레드밀 운동 집단에서는 상쇄되는 경향을 나타냈다. Socio-sexual behavior test 중 Shank3B KO 마우스는 암컷 마우스에 대해 회피하는 행동을 보였으며, Shank3B KO+트레드밀 운동 집단에는 사회적 기피행동이 상쇄되는 것으로 나타났다( Fig. 3B).
Fig. 3.
Fig. 3.Exercise-induced improvement of social interaction deficits in ASD model mice. (A) Time spent sniffing (sec) in a Two-Chamber social behavior test. (B) Time spent nose-nose sniffing (sec), Time spent anus sniffing (sec) in Socio-Sexual behavior test. All values are expressed in the means±SD. * p<.05 versus KO Group; ** p<.05 versus KO Group; ## p<.001 versus KO Group; ### p<.001 versus KO Group; *** p<.001 versus KO Group. 
4. 트레드밀 운동을 통한 SHANK 글루타메이트 수용체 단백질 변화
Western blot을 이용하여 집단 간 전두엽 피질(PFC) 지역에서의 Glutamate receptor 2 (GluR2), Homer1 단백질 발현의 차이를 확인하였다( Fig. 4A). 그룹 간의 단백질 발현 정도의 차이를 GAPDH를 통해 단백질 정량화 하였다. 대조군 집단에 비해 Shank3B KO 집단이 감소된 경향을 볼 수 있으며, Shank3B KO+트레드밀 운동 집단은 Shank3B KO 집단에 비해 증가하는 결과를 확인하였고( Fig. 4B), 대조군 집단에 비해 Shank3B KO 집단이 감소된 경향을 볼 수 있으며, Shank3B KO+트레드밀 운동 집단은 Shank3B KO 집단에 비해 향상된 결과를 확인하였다( Fig. 4C).
Fig. 4.
Fig. 4.Investigation of treadmill exercise on Shank gene-related glutamate receptor protein (A) Representative western blot image of GluR2, and Homer1 (GluR2, Homer1 n=8 per group). (B,C) Densitometry quantification of GluR2 and Homer1. β-actin was probed as the housekeeping gene. All values are expressed in the means±SD. GluR2, Glutamate receptor 2; Homer1, Homer protein homolog 1. Bonferroni post hoc test after ANOVA. 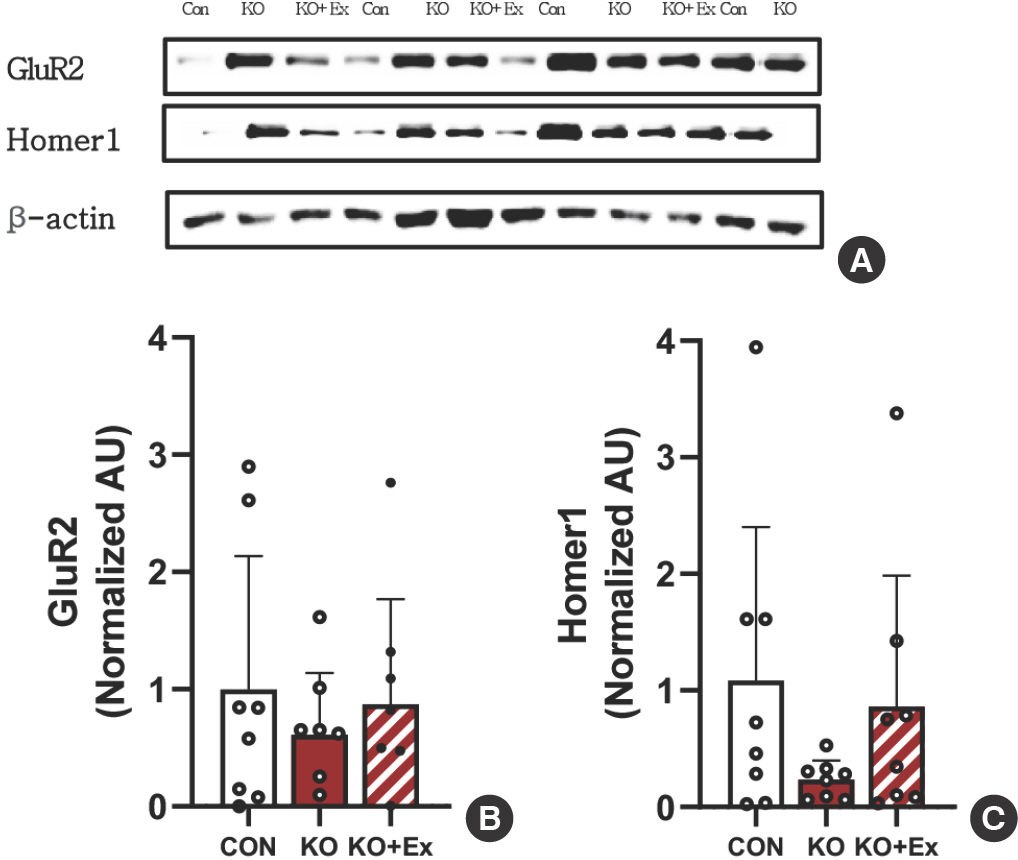
5. 트레드밀 운동을 통한 SHANK 신호전달 단백질의 인산화
Western blot을 이용하여 집단 간 전두엽 피질(PFC) 지역에서의 인산화된(Phopholylated-) PSD95 단백질, GSK-3α/β 단백질, Akt1 단백질 발현의 차이를 확인하였다( Fig. 5A). 그룹 간의 단백질 발현 정도의 차이를 GAPDH, β-actin을 통해 단백질 정량화 하였다. 대조군 집단에 비해 Shank3B KO 집단이 인산화 PSD95가 높게 발현되었으며, 트레드밀 운동을 시킨 Shank3B KO+트레드밀 운동 집단에서는 Shank3B KO 집단에 비해 적게 발현된 결과를 볼 수 있다( Fig. 5B). 인산화 Akt1에서 대조군 집단에 비해 Shank3B KO 집단이 높게 발현되어 있으며, Shank3B KO+트레드밀 운동 집단에서는 대조군 집단보다 더 낮은 경향을 볼 수 있다( Fig. 5C). 인산화 GSK-3α에서 대조군 집단에 비해 Shank3B KO 집단이 높게 발현되어 있으며, Shank3B KO+트레드밀 운동 집단에서는 트레드밀 운동 후 대조군 집단과 비슷한 수준으로 감소되는 경향을 보인다( Fig. 5D). 인산화 GSK-3β에서도 대조군 집단에 비해 Shank3B KO 집단이 높게 발현되어 있으며, Shank3B KO+트레드밀 운동 집단에서 트레드밀 운동 후 대조군 집단과 비슷한 수준으로 감소되는 경향을 보였다( Fig. 5E).
Fig. 5.
Fig. 5.Investigation of treadmill exercise on Shank gene-related phosphor-ylation protein. (A) Representative western blot image of p-PSD95, p-Akt1 and p-GSKα/β (p-PSD95, p-GSK-3α/β n=8 per group; p-Akt1 n=6 per group), (C) Densitometry quantification of p-Akt1. β-actin was probed as the housekeeping gene. (B, D, E) Densitometry quantification of p-PSD95 and p-GSKα/β. GAPDH was probed as the housekeeping gene. All values are expressed in the means±SD. p-PSD95, phosphorylation postsynaptic density protein-95; p-Akt1, phosphorylation serine-threonine protein ki-nase AKT1; p-GSK-3α/β, phosphorylation glycogen synthase kinase-3 α/β. Bonferroni post hoc test after ANOVA. All values are expressed in the means±SD. 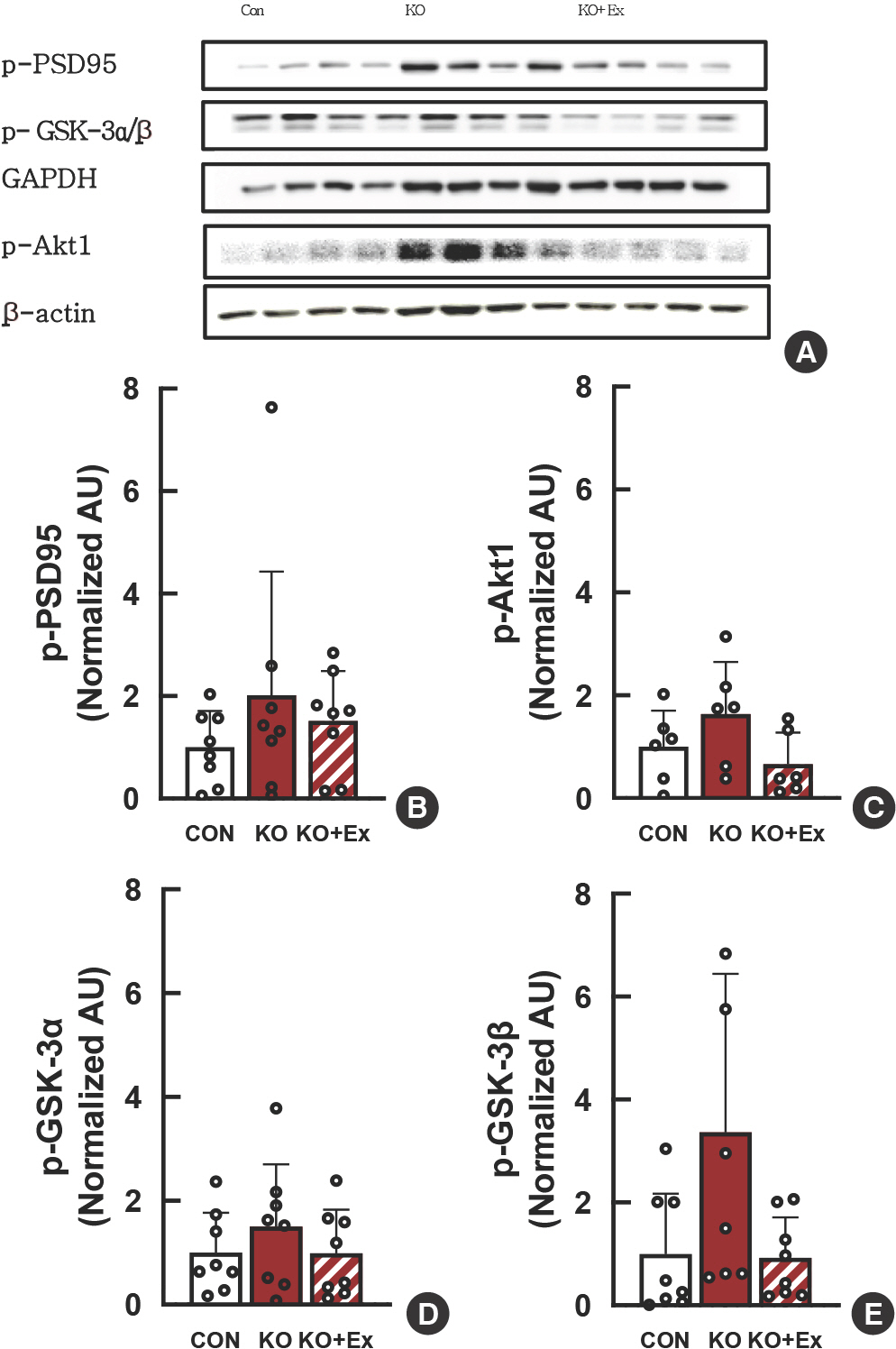
논 의
오늘날 자폐장애 인구의 증가로 인해, 자폐스펙트럼장애(Autism Spectrum Disorders, ASD)의 치료 방법에 많은 노력을 기울이고 있으며, 자폐스펙트럼장애의 유전적 위험의 다양성에 대해 점차 구체화되고 있다[ 31]. 유전적 요인에 따르면 형제나 자매 내에서도 나이가 더 많은 어린이가 자폐스펙트럼장애 발생률 7-20%가 더 높은 것으로 알려지며, 이러한 유병률은 자폐스펙트럼장애를 앓고 있는 남아가 여아보다 3-4배가 더 높은 것으로 나타났다[ 31]. 자폐스펙트럼장애 유전학에 대한 많은 연구가 진행되었음에도 불구하고, 이러한 장애와 관련된 신경생물학적 기질과 신경 회로는 거의 알려지지 않은 상태로 남아있다. Shank3 유전자는 Shank3가 22q13.3 결실 증후군의 주요 원인 유전자임을 시사하는 연구 결과가 늘어나면서 자폐관련 연구모델로 주목되기 시작했다[ 32, 33]. Shank3B KO 마우스를 대상으로 한 선행 연구에서 피질 글루타메이트성 시냅스 구조 및 기능에서 Shank3의 중요한 역할을 밝힐 뿐만 아니라, 유전자의 변형과 마우스의 자폐증 유사 행동 발달 사이의 연관성을 보여주었다[ 34]. 자신의 신체 표면을 관리하는 그루밍 행동은 일반적으로 발생하는 마우스의 자발적인 행동 중 하나이며, 자폐스펙트럼장애의 흔한 증상 중 하나인 반복적인 행동은 인간을 포함한 대부분의 동물에서 나타나는 행동으로 알려진다[ 35]. Sigoli et al. [ 30]의 선행 연구에서 트레드밀 운동 방법을 통해 좋은 결과를 나타내지 못하여 스트레스에 취약한 자폐스펙트럼장애 모델 Shank3B KO 마우스에서 운동 방법을 강도와 기간을 조절하여 트레드밀 운동을 실시하였다. 트레드밀 운동 후 자폐스펙트럼장애 모델 Shank3B KO 마우스에서 반복적인 행동인 Self-grooming 행동 실험에서 대조군 집단에 비해 Shank3B KO 집단이 과한 그루밍 행동을 보였으며( Fig. 2A), Shank3B KO+트레드밀 운동 집단에서 그루밍 행동이 감소된 결과를 볼 수 있었다. 이는 트레드밀 운동으로 인해 반복적인 행동 개선의 긍정적인 효과를 나타냄을 시사한다. 자폐스펙트럼장애의 다른 유전자 모델에서는 유전적 변형된 동물이 어미와의 사회적 의사소통에 이상을 보이는 것으로 나타났으며, 이는 기능적으로 자폐스펙트럼장애의 병인과 밀접한 관련이 있음을 나타냈다[ 19]. 사회적 상호작용 결함 실험을 나타내는 Two-chamber so-cial behavior test에서 표적 마우스가 들어있는 원통 케이지에서의 스니핑 시간은 대조군 집단과 Shank3B KO 집단, Shank3B KO+트레드밀 운동 집단 간의 유의한 차이가 나타났다( Fig. 3A). 트레드밀 운동의 효과는 반복적인 행동이나 사회적 상호작용 결함에 대한 개선 방안에 긍정적인 영향을 나타내는 것으로 보여진다. Socio-sexual behavior test 인 수컷-암컷과의 사회적 상호작용 실험에서 대조군 집단과 Shank3B KO 집단 간의 유의한 차이가 나타났으며, Shank3B KO+트레드밀 운동 집단에서 사회적 상호작용 결함 행동이 개선된 것을 볼 수 있다 ( Fig. 3B). 이러한 행동학적 결과로 보아, 11주령 Shank3B KO 수컷 마우스에서 트레드밀 운동으로 인해 반복적인 행동과 사회적 상호작용 결함을 완화할 수 있는 가능성을 보여주고 있으며, 자폐 행동 장애로 나타나는 추가적인 행동 개선 효과에 대한 연구의 필요성을 가지고 있음을 시사한다. 행동학적인 결과는 신경 발달의 결함에 기반한다고 볼 수 있다. 마우스의 그루밍 행동이 나타나는 원인은 피질의 시냅스 결함이라고 예측되고, 이로 인한 신경 회로의 활성화를 조절하여 그루밍 행동을 보인다고 알려진다. 따라서 그루밍 행동을 조절하는 신경학적 변화가 유전적으로 영향을 미친다는 것을 보여준다. 운동은 근육 사용의 증가 또는 감소에 따른 운동 시스템을 통해 뉴런의 기능과 조절에 상당한 변화가 나타나는 것으로 알려져 있다. 또한 수용체의 유전자 발현과 뉴로트로핀의 단백질 합성을 조절하여 신경 흥분성을 증가시키고 수지상 성장과 가소성을 확장시키는 신경 형태의 변화를 일으킨다[ 36]. 발달 전반에 걸쳐 SHANK 단백질은 주로 선조체, 해마, 소뇌 및 피질과 같은 다양한 뇌 영역에서 발현되며, 모두 감각 운동 기능과 인지 기능에 중추적인 역할을 한다[ 34, 37]. 선조체의 기능 장애로 인한 촉각 및 시각적 자극을 통해 감각운동 활동에 문제가 발생하여 Shank3B KO 마우스가 인식하는 데 어려움을 겪게 된다[ 37]. Carol et al. [ 38] 선행 연구에 의하면 시냅스 기능 장애는 만성 질환에서 인지 상실의 주요원인으로 바라보고 있으며, 인슐린 수용체의 역할과 연관성을 보였다. 인슐린과 관련있는 IRSp53은 Shank3와 피질과 해마, 소뇌에서 발견하였으며, 위의 선행 연구의 기반으로 피질에 초점을 두었다. 동시에 SHANK 단백질의 세포 신호전달에 관여하는 GluR2, Homer1에서 대조군 집단과 Shank3B KO 집단 간의 차이가 났으며( Fig. 4A, B), 이는 자폐스펙트럼장애 동물 모델인 Shank3B KO 마우스에서 글루타메이트 수용체의 결함이 있다는 것을 나타낸다. Shank3B KO+트레드밀 운동 집단의 전두엽 피질 지역에서 GluR2는 Shank3B KO 집단에 비해 단백질 발현이 향상된 것을 볼 수 있었으며, Homer1도 Shank3B KO 집단에 비해 Shank3B KO+트레드밀 운동 집단이 향상된 결과를 볼 수 있다. 이는 트레드밀 운동이 SHANK 단백질 발현 개선에 긍정적인 영향을 미친다는 것을 시사한다. SHANK 단백질은 여러 단백질 복합체 및 세포골격 요소와 상호 작용하는 역할로 인해 PSD의 구성요소로 알려진다. SHANK의 5개 do-main은 PSD에 대한 스캐폴딩을 형성하며, Postsynaptic에서 AMPA 수용체는 SHANK PDZ domain과 직접적으로 상호작용하는 글루타메이트 수용체 AMPA 결합 단백질(ABP)에 의해 형성된다. SHANK는 Homer-mGluR 수용체 복합체와 PSD-95/GKAP-NMDA 수용체를 형성하며, Homer1은 칼슘과 칼륨 채널과도 상호작용을 한다[ 38]. GSK-3α/β는 뇌에 풍부한 세린/트레오닌 키나제이며, 세포 과정 및 신호 전달 경로, 특히 시냅스 발달 및 가소성과 밀접한 관련이 있다[ 29]. GSK-3α/β 는 NMDA 수용체와 PSD95를 인산화하여 글루탐산 시냅스의 기능을 조절하며, GSK3 family의 인산화로 인해 AKT, RICTOR, TSC1 및 PTEN, IRS1, IRIS2를 포함하여 P13K/AKT/mTOR 신호 전달네트워크를 조절하는 것으로 알려진다[ 39]. Shank3B KO 선조체에서 약간 감소하거나 변화가 없는 선행 연구에 비해, 본 연구의 인산화 PSD95가 대조군 집단에 비해 Shank3B KO 집단이 상승된 결과를 나타내는 것으로 보아, 전두엽 피질 지역 이외의 다른 지역에서 인산화 PSD95의 발현 정도의 차이에 대해서는 추가적인 연구가 필요할 것으로 보여진다( Fig. 5B). 본 연구 결과에서 인산화 GSK-3α와 인산화 GSK-3β는 대조군 집단에 비해 Shank3B KO 집단이 감소하는 경향을 볼 수 있었으며, Shank3B KO+트레드밀 운동 집단에서는 대조군 집단과 비슷한 수준으로 회복되는 것을 확인하였다( Fig. 5D, E). 이는 전두엽 피질 지역에서의 SHANK 글루타메이트 수용체 시냅스에서 트레드밀 운동으로 인하여 인산화 GSK-3α/β의 기능이 회복이 되었음을 알 수 있다. 또한 GSK-3α/β 활성을 조절하는 인산화 Akt1 단백질이 대조군 집단에 비해 Shank3B KO 집단에서 높게 발현이 되었으며( Fig. 5C), 이 또한 트레드밀 운동을 통해 대조군 집단처럼 낮아진 경향을 볼 수 있다. 이외에도 SHANK 구조 단백질 중 하나인 카테닌은 ShankB KO의 전두엽 피질에서 활성화가 되고, GSK-3β를 국소적으로 활성화 시켰을때, 시냅스 발달과 사회적 결함 기능의 개선된다는 것을 보여주었다[ 29]. 따라서, 트레드밀 운동이 뉴런 시냅스에서 인산화 단백질을 변화하는 경로에 관여하는 단백질을 포함하여, 후속 연구에서 SHANK 단백질의 기전과 변화, 세부적인 요인 등을 구체화한 연구를 통해 트레드밀 운동의 효과를 더욱 명확히 규명할 필요가 있다. 트레드밀 운동은 자폐 행동 개선을 가져오며, SHANK 조절 수용체인 GluR2와 Homer1, 하위 신호전달 물질인 GSK-3α/β, Akt1의 인산화에 긍정적인 처치방법으로, 향후 자폐스펙트럼장애에서 운동 치료는 자폐행동 개선을 중심으로 한 연구 분야의 기초자료로서 의미 있는 정보를 제공할 것으로 판단된다.
결 론
트레드밀 운동은 자폐스펙트럼장애(Autism Spectrum Disorder, ASD) 모델 마우스의 반복적인 행동이나 사회적 상호작용 결함에 대한 행동학적 변화에 긍정적인 영향을 미쳤으며, 자폐스펙트럼장애 기전을 조절하는 SHANK 글루타메이트 수용체와 SHANK 하위 신호전달물질인 단백질의 인산화에 변화를 보일 수 있음을 확인하였다. 이는 트레드밀 운동 처치가 자폐스펙트럼장애의 자폐행동 개선 및 신경 시냅스 조절에 효과적인 방안임을 시사한다. 추후, 후속 연구에서 SHANK 단백질을 구성하는 요소들의 변화 및 세부적인 하위조절 요인 등의 국소적 조절 등을 구체화한 연구를 통해 트레드밀 운동의 효과를 더욱 명확히 규명할 필요성이 있다고 사료된다.
REFERENCES
1. American Psychiatric Association D, American Psychiatric Association. Diagnostic and statistical manual of mental disorders: DSM-5 (Vol. 5, No. 5). Washington, DC: American psychiatric association; 2013.
3. Newschaffer CJ, Croen LA, Daniels J, Giarelli E, Grether JK, et al. The epidemiology of autism spectrum disorders. Annu Rev Public Health. 2007;28:235-58.   6. Autism and developmental disabilities monitoring network surveil-lance year 2008 principal investigators; centers for disease control and prevention. Prevalence of autism spectrum disorders-Autism and De-velopmental Disabilities Monitoring Network, 14 sites, United States, 2008. MMWR Surveill Summ. 2012;61(3):1-19.
7. DeFilippis M, Wagner KD. Treatment of autism spectrum disorder in children and adolescents. Psychopharmacol Bull. 2016;46(2):18-41.   11. Bearss K, Johnson C, Smith T, Lecavalier L, Swiezy N, et al. Effect of parent training vs parent education on behavioral problems in children with autism spectrum disorder:a randomized clinical trial. JAMA. 2015;313(15):1524-33.  12. Silk TJ, Rinehart N, Bradshaw JL, Tonge B, Egan G, et al. Visuospatial processing and the function of prefrontal-parietal networks in autism spectrum disorders:a functional MRI study. Am J Psychiatry. 2006;163(8):1440-3.  13. Horwitz B, Rumsey JM, Grady CL, Rapoport SI. The cerebral meta-bolic landscape in autism. Intercorrelations of regional glucose utilization. Arch Neurol. 1988;45(7):749-55.   14. Sears LL, Vest C, Mohamed S, Bailey J, Ranson BJ, et al. An MRI study of the basal ganglia in autism. Prog Neuropsychopharmacol Biol Psychiatry. 1999;23(4):613-24.  16. Lutz AK, Pfaender S, Incearap B, Ioannidis V, Ottonelli I, et al. Autism-associated SHANK3 mutations impair maturation of neuromuscular junctions and striated muscles. Sci Transl Med. 2020;12(547):eaaz3267.   23. Irie M, Hata Y, Takeuchi M, Ichtchenko K, Toyoda A, et al. Binding of neuroligins to PSD-95. Science. 1997;277(5331):1511-5.   35. Fentress JC. Expressive contexts, fine structure, and central mediation of rodent grooming. Ann N Y Acad Sci. 1988;525:18-26.  36. Dai Y, Cheng Y, Ge R, Chen K, Yang L. Exercise-induced adaptation of neurons in the vertebrate locomotor system. J Sport Health Sci. 2023;31:S2095-2546(23)00104-7.   39. Hermida MA, Dinesh Kumar J, Leslie NR. GSK3 and its interactions with the PI3K/AKT/mTOR signalling network. Adv Biol Regul. 2017;65:5-15.  
|
|










